(每空2分 共16分)依据事实 填空:(1)在25℃ 101kPa下 1g甲醇液体完全燃烧生成CO2
| (每空2分,共16分)依据事实,填空: (1)在25℃、101kPa下,1g甲醇液体完全燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为_____________________________ (2)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为_________________ (3)氢氧燃料电池已用于航天飞机。以30%KOH溶液为电解质的这种电池在使用时的电极反应式: 正极: ;负极: (4)在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
(5)某核素AZX的氯化物XCl2 1.11 g配成溶液后,需用1mol·L-1的硝酸银溶液20 ml才能把氯离子完全沉淀下来。则X的质量数为 ;若X的核内中子数为20,则37 g XCl2中所含质子的物质的量 。 |
参考解答
(1) CH3OH(l)+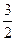 O2(g)→CO2(g)+2H2O(l) ΔH=–725.76kJ·mol-1 O2(g)→CO2(g)+2H2O(l) ΔH=–725.76kJ·mol-1(2)N2(g)+3H2(g)=2NH3(g) ΔH=-92kJ·mol-1 (3)O2+2H2O+4e-==4OH- 2H2+4OH--4e-==4H2O (4) X+3Y 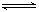 2Z 75% 2Z 75%(5) 40 ; 18mol |
| 略 |
相似问题
(8分)一定温度下将3molA和1molB气体通入体积为2L的密闭恒容容器中 发生反应3A(g)+
(8分)一定温度下将3molA和1molB气体通入体积为2L的密闭恒容容器中,发生反应3A(g)+ B(g)xC(g)2min时反应平衡,剩余0 8molB,并测得C的浓度为0 4mol L
(12分)(1)在密闭容器里 通入x mol SO2和y mol O2 发生化学反应:2SO2 (g
(12分)(1)在密闭容器里,通入x mol SO2和y mol O2,发生化学反应:2SO2 (g) + O2 (g)2SO3 (g) ;当其它条件不变时,改变下列条件,反应
对于处于化学平衡状态的反应CO(g)+H2O(g)? CO2(g)+H2(g) 若要提高CO的转化
对于处于化学平衡状态的反应CO(g)+H2O(g)?CO2(g)+H2(g),若要提高CO的转化率,下列措施中可行的是()A.升温B.增大H2O(g)的浓度C.增大压强D.使用合适的催化剂
甲溶液的pH是4 乙溶液的pH是5 甲溶液与乙溶液的c(H+)之比为A. 10:1
甲溶液的pH是4,,乙溶液的pH是5,甲溶液与乙溶液的c(H+)之比为A 10:1 B 1:10 C 2:1 D1:2
运用化学反应原理研究氮 氧 镁 铜等元素及其化合物的性质。⑴合成氨反应反应:N2(g)+3H2(g)
运用化学反应原理研究氮、氧、镁、铜等元素及其化合物的性质。⑴合成氨反应反应:N2(g)+3H2(g)2NH3(g),ΔH=-QkJ mol。若在恒温、恒压条件下向平衡体系中












