粗盐经溶解 过滤将不溶杂质除去 得到较纯的盐M.盐M中仍含有少量的可溶性杂质氯化钙和氯化镁.为除去盐
粗盐经溶解、过滤将不溶杂质除去,得到较纯的盐M.盐M中仍含有少量的可溶性杂质氯化钙和氯化镁.为除去盐M中含有的氯化钙和氯化镁,某同学设计了如下实验进行探究: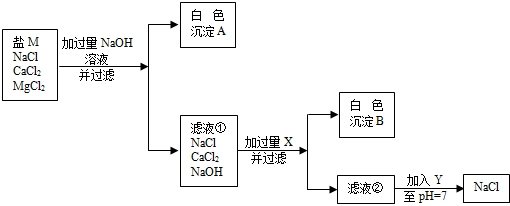 物质的溶解性,可查阅第20题中“部分酸、碱、盐的溶解性表(20℃)”(本题将“微溶”当成“可溶”),观察上图后回答以下问题 (1)加入过量的NaOH的目的是______,Y是______(填化学式) (2)滤液②中的溶质是______.(填化学式) (3)生成白色沉淀B的化学方程式是______.滤液②加入调至pH=7时的化学反应方程式是______. |
参考解答
| (1)钠离子形成的化合物都溶于水,氢氧根离子会与镁离子生成氢氧化镁沉淀,在除去镁离子和钙离子时,加入的氢氧化钠和碳酸钠都是过量的,对于氯化钠也是杂质,需要将两者转化为氯化钠,故答案为:除去Mg2+,HCl; (2)加入过量的氢氧化钠反应后生成氢氧化镁沉淀和氯化钠,加入过量的碳酸钠后生成碳酸钙沉淀和氯化钠,过滤后溶液中就剩下氯化钠、氢氧化钠、和碳酸钠, 故答案为:NaOH、NaCl、Na2CO3; (3)碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,故答案为:Na2CO3+CaCl2═CaCO3↓+2NaCl; 盐酸和氢氧化钠反应生成氯化钠和水,盐酸和碳酸钠反应生成氯化钠、水和二氧化碳,故答案为:HCl+NaOH═NaCl+H2O、Na2CO3+2HCl═2NaCl+H2O+CO2↑; |
相似问题
如图是粗盐除杂提纯得到较纯净的氯化钠固体的过程.(此题中微溶物视为可溶物)请回答下列问题:(1)上述
如图是粗盐除杂提纯得到较纯净的氯化钠固体的过程.(此题中微溶物视为可溶物)请回答下列问题:(1)上述过程中的某操作是指______;(2)A溶液是______
我们通常所说的家用调味品盐和化学上的盐是一回事吗?
我们通常所说的家用调味品盐和化学上的盐是一回事吗?
利用右图装置可完成多种实验.回答下列问题:(1)写出图中标号仪器的名称:a.______ b.___
利用右图装置可完成多种实验.回答下列问题:(1)写出图中标号仪器的名称:a.______b.______c.______(2)利用该实验装置可完成H2还原CuO及CO还原CuO
如图是用海水提取粗盐的大致过程.下列说法错误的是( )A.海水进入贮水池 海水的成分基本不变B.析
如图是用海水提取粗盐的大致过程.下列说法错误的是( )A.海水进入贮水池,海水的成分基本不变B.析出晶体后的母液是氯化钠的不饱和溶液C.在蒸发池
一氧化碳气体在生产生活中有着广泛的应用。 (1) 下列对一氧化碳的有关描述 错误的是_____(
一氧化碳气体在生产生活中有着广泛的应用。(1) 下列对一氧化碳的有关描述,错误的是_____( 填序号) 。 A 组成:由碳原子和氧原子组成 B 性质:能












