20℃时 取相同质量的a b c三种物质的饱和溶液分别置于三个烧杯中 再分别向其中加入相同质量的相应
20℃时,取相同质量的a,b,c三种物质的饱和溶液分别置于三个烧杯中,再分别向其中加入相同质量的相应固体溶质,将温度升高到40℃,固体的溶解情况如图1所示.图2为a,b,c三种物质的溶解度曲线.请仔细阅读图1和图2回答下列问题: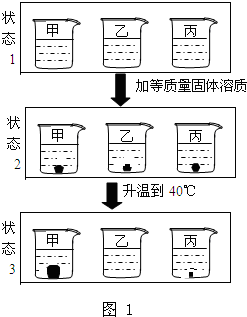 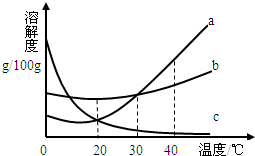 (1)三种物质的溶解度关系为b>a>c时的温度为t,则t的取值范围是______. (2)烧杯甲里是______(填“a”“b”或“c”)物质的溶液. (3)40℃时,烧杯______(填“甲”、“乙”或“丙”)里的溶液中溶剂最小. (4)下列各种状态下,各烧杯(甲、乙、丙)里的溶液中溶质的质量分数的比较中一定正确的是______. A.甲(状态2)>甲(状态1)B.乙(状态1)>甲(状态3) C.甲(状态1)=乙(状态2)D.乙(状态3)>丙(状态3) |
参考解答
| (1)根据三种物质的溶解度曲线不难看出,在20℃~30℃时,三种物质的溶解度关系为b>a>c,故答案为:20~30℃ (2)由于烧杯甲中的溶液温度越高,烧杯中的晶体越多,说明该物质的溶解度随温度的升高而减小,因此该物质应为c (3)由于在一系列的变化中溶剂的质量并没有发生变化,因此比较原来的溶剂多少即可;由于在20℃时,三物质的溶解度大小关系为b>a=c,则其饱和溶液中溶质的质量分数大小关系为b>a=c,则等量的饱和溶液中溶质的质量b>a=c,则溶剂的质量b<a=c,而b的溶解度受温度的影响最小,因此应是丙中的物质,故答案为:丙 (4)由于加入的是等质量的物质进行溶解,根据溶解现象,当温度升高到40℃时,甲中固体增多,说明甲中溶质为C,而乙中固体无剩余,说明温度对溶解度影响较大,应该是为a,丙中固体减少,但是不是很明显,所以是受温度影响不大的b物质. A.由于是在温度不变的情况下,向饱和溶液中加入一定的溶质,因此溶液中溶质的质量分数不会发生变化,故A错误; B.由于甲中盛放的是c,而乙中盛放是a,在20℃时,c的溶解度等于a,则饱和溶液中溶质的质量分数a=c,由于c的溶解度随温度的升高而减小,因此升温后c的溶液中会有晶体析出,溶质的质量分数会减小,故B正确; C.由于在20℃时,c的溶解度等于a,则饱和溶液中溶质的质量分数a=c,向乙中加入一定量的b即向b的饱和溶液中加入一定的b,因此溶质不会继续溶解,因此溶质的质量分数不会发生变化,故C正确; D.由于在20℃时,a和b的溶解度大小关系是b>a,因此其饱和溶液中溶质的质量分数大小关系也是b>a,当向它们的等量饱和溶液中加入等量的溶质后并升温后,乙中的a全部溶解,而丙中的b只溶解了一部分,因此所得溶液中溶质的质量分数无法判断大小,故D错误; 故选BC. |
相似问题
右图是A B C三种物质的溶解度曲线 我能根据此图回答下列问题:(1)______℃时 物质A和C的
右图是A、B、C三种物质的溶解度曲线,我能根据此图回答下列问题:(1)______℃时,物质A和C的溶解度相等;(2)等质量的A、B、C三种物质的饱和溶液同时
已知X物质与Y物质的溶解度都随温度的升高而增大 20℃时 10g水中最多溶解4g X物质 30℃时
已知X物质与Y物质的溶解度都随温度的升高而增大,20℃时,10g水中最多溶解4gX物质,30℃时,20g水中最多溶解8gY物质,则20℃时X与Y的溶解度相比是(
20℃时 NaCl的溶解度为36g 5克NaCl放入到20克水中得到溶液的质量为______ 克.1
20℃时,NaCl的溶解度为36g,5克NaCl放入到20克水中得到溶液的质量为______克.10克NaCl放入到20克水中,得到溶液的质量为______.100mL酒精和100mL水混
如图是A B C三种物质的溶解度曲线:请回答:(1)t1℃时 A B C三种物质中溶解度最大的是__
如图是A、B、C三种物质的溶解度曲线:请回答:(1)t1℃时,A、B、C三种物质中溶解度最大的是______:(2)在t1℃时,将25gA物质加入到盛有50g水的烧杯中
下列加速固体物质溶解的措施中 能改变固体物质的溶解度的有( )A.加热B.把固体研细C.搅拌D.振
下列加速固体物质溶解的措施中,能改变固体物质的溶解度的有( )A.加热B.把固体研细C.搅拌D.振荡












