质量守恒定律的内容为:“在化学反应中 参加反应的各物质的质量总和 等于反应后生成各物质的质量总和”.
| 质量守恒定律的内容为:“在化学反应中,参加反应的各物质的质量总和,等于反应后生成各物质的质 量总和”. 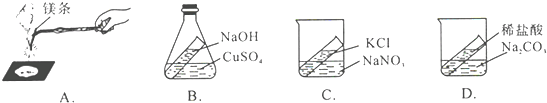 (1)有气体参加、有气体生成的反应,一般不能用于直接验证质量守恒定律,如上图中的______. (2)没有发生化学反应的,也不能用于验证质量守恒定律,如上如中的C.C烧杯中两种物质不发生化学反应的理由是______. (3)写出B装置中发生反应的化学方程式______. |
参考解答
| (1)有气体参加、有气体生成的反应,一般不能用于直接验证质量守恒定律,镁条燃烧有氧气参加反应,稀盐酸和碳酸钠反应生成二氧化碳气体,因此上图中的AD不能用于直接验证质量守恒定律,故答案为;AD; (2)氯化钾、硝酸钠两种物质相互交换成分不生成气体或沉淀或水,因此两者不发生化学反应,故答案为:氯化钾、硝酸钠两种物质相互交换成分不生成气体或沉淀或水. (3)氢氧化钠溶液和硫酸铜溶液反应生成氢氧化铜沉淀和硫酸钠,反应的化学方程式为:2NaOH+CuSO4=Na2SO4+Cu(OH)2↓.故答案为:2NaOH+CuSO4=Na2SO4+Cu(OH)2↓. |
相似问题
已知:反应3A+2B=2C+D A B两物质完全反应时的质量比为3:4 若生成C和D共140g 则该
已知:反应3A+2B=2C+D,A、B两物质完全反应时的质量比为3:4,若生成C和D共140g,则该反应消耗B的质量为( )A.60gB.80gC.90gD.120g
下列叙述中正确的是( )A.4g氢气和8g氧气混合 点燃后充分反应生成12g水B.3g碳在空气中完
下列叙述中正确的是( )A.4g氢气和8g氧气混合,点燃后充分反应生成12g水B.3g碳在空气中完全燃烧,生成11g二氧化碳,参加反应的氧气的质量为8gC.煤
在4Al+3O2═2Al2O3的反应中 反应前后肯定发生变化的是( )A.元素种类B.各种原子的数
在4Al+3O2═2Al2O3的反应中,反应前后肯定发生变化的是( )A.元素种类B.各种原子的数目C.物质的质量总和D.各元素的化合价
在2Mg+O2 点燃 . 2MgO的反应中 参加反应的氧气的质量和生成的氧化镁的质量关系( )A.
在2Mg+O2点燃 2MgO的反应中,参加反应的氧气的质量和生成的氧化镁的质量关系( )A.氧气的质量<氧化镁的质量B.氧气的质量>氧化镁的质量C.氧气的
某纯净物M在隔绝空气加热时分解为氧化铜 二氧化碳 水.根据上述实验事实能得出的结论是( )A.M由
某纯净物M在隔绝空气加热时分解为氧化铜、二氧化碳、水.根据上述实验事实能得出的结论是( )A.M由四种元素组成B.M是氧化物C.M中含水D.M是单质












