向含有Fe2+ I- Br-的溶液中通入适量氯气 溶液中各种离子的物质的量变化曲线如图所示.有关说法
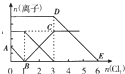
向含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离子的物质的量变化曲线如图所示.有关说法不正确的是( )
 |
参考解答
| 还原性I->Fe2+>Br-,故首先发生2I-+Cl2═I2+2Cl-,I-反应完毕再发生:2Fe2++Cl2═2Fe3++2Cl-;最后发生反应2Br-+Cl2═Br2+2Cl-, A.B点时溶液中I-完全反应,溶液中存在Fe2+和Br-,BC段发生2Fe2++Cl2═2Fe3++2Cl-,代表Fe3+的物质的量的变化情况,故A正确; B.由图可知,BC段发生2Fe2++Cl2═2Fe3++2Cl-,Fe2+反应完毕消耗氯气2mol,由方程式可知n(Fe2+)=2×2mol=4mol,无法得到原溶液的体积,故不能计算原混合溶液中c(FeBr2),故B错误; C.AB段发生2I-+Cl2═I2+2Cl-,2mol的I-消耗1mol氯气,BC段发生2Fe2++Cl2═2Fe3++2Cl-,余下的1mol氯气再与2molFe2+反应,故参加反应的n(Fe2+):n(I-)=1:1,故通入2molCl2时,溶液中已发生的离子反应可表示为2Fe2++2I-+2Cl2═2Fe3++I2+4Cl-,故C正确; D.由图可知AB段消耗氯气1mol,发生2I-+Cl2═I2+2Cl-,故n(I-)=2n(Cl2)=2mol,BC段发生2Fe2++Cl2═2Fe3++2Cl-,消耗氯气2mol,故n(Fe2+)=2n(Cl2)=2×2mol=4mol,DE段发生2Br-+Cl2═Br2+2Cl-,消耗氯气3mol,故n(Br-)=2n(Cl2)=6mol,故原溶液中n(Fe2+):n(I-):n(Br-)=4mol:2mol:6mol=2:1:3,故D正确; 故选B. |
相似问题
下列各反应的离子方程式中 正确的是( )A.硫酸铝溶液中加入过量的氨水:Al3++3OH-═Al(
下列各反应的离子方程式中,正确的是( )A.硫酸铝溶液中加入过量的氨水:Al3++3OH-═Al(OH)3B.铜与氯化铁溶液反应:Cu+Fe3+═Cu2++Fe2+C.NaHCO3
现有Ca(OH)2 Na2CO3 BaCl2 NaOH 盐酸 稀硫酸六种溶液 它们存在如图所示的相互
现有Ca(OH)2、Na2CO3、BaCl2、NaOH、盐酸、稀硫酸六种溶液,它们存在如图所示的相互反应关系,图中每条线两端的物质可以发生化学反应,试回答下列问题
下列离子方程式中书写正确的是( )A.盐酸与碳酸钙反应:CO32-+2H+═CO2↑+H2OB.氯
下列离子方程式中书写正确的是( )A.盐酸与碳酸钙反应:CO32-+2H+═CO2↑+H2OB.氯化铝溶液中加入足量的氨水:Al3++3NH3?H2O═Al(OH)3↓+3NH4+C.
向等体积等物质的量浓度的NaCl MgCl2两溶液中分别滴加等浓度的AgNO3溶液使Cl-恰好沉淀完
向等体积等物质的量浓度的NaCl、MgCl2两溶液中分别滴加等浓度的AgNO3溶液使Cl-恰好沉淀完全,则消耗AgNO3溶液的体积之比为( )A.1:1B.1:2C.2:1D.1:3
下列方程式正确的是 [ ]A.过量的铁粉放入稀HNO3中:Fe+4H++NO3-= Fe3+
下列方程式正确的是 [ ]A.过量的铁粉放入稀HNO3中:Fe+4H++NO3-=Fe3++NO↑+2H2O B.过量的铁粉在氯气中燃烧:Fe+Cl2FeCl2 C.适量的SO2通入到Ba(NO












