在1 L含0.1 mol NaAlO2和0.1 mol Ba(OH)2的混合溶液中 逐滴加入浓度为0
在1 L含0.1 mol NaAlO2和0.1 mol Ba(OH)2的混合溶液中,逐滴加入浓度为0.1 mol·L-1H2SO4溶液,下列图像中能表示反应产生沉淀的物质的量与加入硫酸溶液体积之间关系的是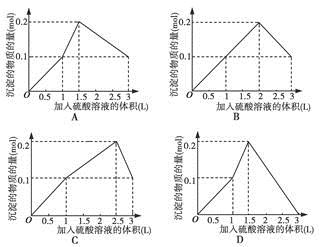 |
参考解答
| A |
混合溶液中加入H2SO4,首先发生Ba(OH)2+H2SO4=BaSO4↓+2H2O,0.1 mol H2SO4刚好与0.1 mol Ba(OH)2完全反应生成0.1 mol BaSO4沉淀,且H2SO4电离出的H+与Ba(OH)2电离出的OH-也刚好完全中和,再加入H2SO4,则发生反应: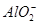 +H++H2O=Al(OH)3↓,即加入0.5 mol H2SO4时生成Al(OH)3为0.1 mol,继续加入H2SO4,则Al(OH)3会溶解,最终只有BaSO4沉淀。 +H++H2O=Al(OH)3↓,即加入0.5 mol H2SO4时生成Al(OH)3为0.1 mol,继续加入H2SO4,则Al(OH)3会溶解,最终只有BaSO4沉淀。 |
相似问题
下列反应属于氧化还原反应的是[ ]A.漂白粉吸收空气中的二氧化碳 B.用萤石和浓硫酸制取氟化
下列反应属于氧化还原反应的是[ ]A 漂白粉吸收空气中的二氧化碳 B 用萤石和浓硫酸制取氟化氢 C 氯水使有色布条褪色 D 黑白照片的底片在相机里曝光时的反应
类推思维是化学解题中常用的一种思维方法 下列有关反应方程式的类推正确的是( ) 已知类推A将Fe加入
类推思维是化学解题中常用的一种思维方法,下列有关反应方程式的类推正确的是()已知类推A将Fe加入CuSO4溶液中:Fe+Cu2+=Cu+Fe2+将Na加入到CuSO4溶
下列褪色过程不是因为氧化还原反应而褪色的是[ ]A.SO2气体通入溴水使溴水褪色 B.氯水使
下列褪色过程不是因为氧化还原反应而褪色的是[ ]A.SO2气体通入溴水使溴水褪色 B.氯水使滴有酚酞的NaOH溶液褪色,加入NaOH后不变红C.将苯滴入溴水中
(1)通常用小苏打的悬浊液除去CO2中的HCl 反应的离子方程式为:
(1)通常用小苏打的悬浊液除去CO2中的HCl,反应的离子方程式为:,不能用NaOH溶液的原因是,也不能用Na2CO3的原因是(均用离子方程式表示原因)(2) 把
向FeCl3 Al2(SO4)3的混合溶液中逐滴加入Ba(OH)2(aq) 形成沉淀的情况如下图所示
向FeCl3、Al2(SO4)3的混合溶液中逐滴加入Ba(OH)2(aq),形成沉淀的情况如下图所示。沉淀的生成与溶解的pH列于下表。以下推断正确的是()氢氧化物溶液pH开












