向FeI2 FeBr2的混合溶液中通入适量氯气 溶液中某些离子的物质的量变化如图所示.已知:2Fe2
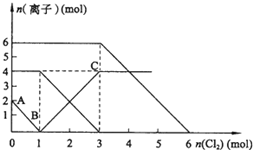
向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.已知:2Fe2++Br2═2Fe3++2Br-;2Fe3++2I-═2Fe2++I2.则下列有关说法中,不正确的是( )
 |
参考解答
| A.反应2Fe2++Br2=2Fe3++2Br-中,还原剂Fe2+的还原性强于还原产物Br-,所以还原性:Fe2+>Br-,反应2Fe3++2I-=2Fe2++I2中,还原剂I-的还原性强于还原产物Fe2+,所以还原性:I->Fe2+,所以还原性I->Fe2+>Br-,故A正确; B.通入氯气后,碘离子先被氧化,其次是亚铁离子,最后是溴离子,在通入氯气的量为0~1mol的过程中,碘离子从最大量降到0,即得到碘离子的物质的量为2mol,通入氯气的量为1~3mol的过程中,亚铁离子从4mol降到0,三价铁的量逐渐增大,所以含有亚铁离子共4mol,在通入氯气的量为3~6mol的过程中溴离子从6ml降到0,所以溴离子的物质的量 是6mol,即FeBr2的物质的量为3mol,故B错误; C.当通入2molCl2时,2mol的I-消耗氯气1mol,余下的1mol氯气再与2molFe2+反应,即溶液中发生的离子反应可表示为2Fe2++2I-+2Cl2=2Fe3++I2+4Cl-,故C正确; D.由B可知,碘离子的物质的量为2mol,亚铁离子是4mol,溴离子的物质的量是6mol,n(Fe2+):n(I-):n(Br-)=2:1:3,故D正确. 故选B. |
相似问题
著名化学家徐光宪获得国家最高科学技术奖 以表彰他在稀土萃取理论方面作出的贡献.已知:金属铈(稀土元素
著名化学家徐光宪获得国家最高科学技术奖,以表彰他在稀土萃取理论方面作出的贡献.已知:金属铈(稀土元素)在空气中易氧化变暗,受热时燃烧,遇水很快
在一定条件下 下列微粒的还原性顺序为Cl-<Br-<Fe2+<I-<SO2 由此判断以下各反应在溶液
在一定条件下,下列微粒的还原性顺序为Cl-<Br-<Fe2+<I-<SO2,由此判断以下各反应在溶液中不能发生的是 [ ]A.2Fe3+ + SO2 + 2H2O == 2Fe2+
在常温下发生下列反应: (1)16H++10Z-+2XO4-=2X2++5Z2+8H2O (2)2A
在常温下发生下列反应: (1)16H++10Z-+2XO4-=2X2++5Z2+8H2O (2)2A2++B2=2A3++2B- (3)2B-+Z2=B2+2Z- 根据上述反应,判断下列结论中错误的是[ ]A.溶
已知氧化性BrO3->ClO3->Cl2>IO3->I2。现将饱和氯水逐滴滴入KI淀粉溶液中至过量。
已知氧化性BrO3->ClO3->Cl2>IO3->I2。现将饱和氯水逐滴滴入KI淀粉溶液中至过量。 (1)可观察到的现象是:①________________________;②_______________
下列微粒中 还原性最强的是( )A.F-B.Cl-C.Br-D.I-
下列微粒中,还原性最强的是( )A.F-B.Cl-C.Br-D.I-












