传统的自来水处理剂是在自来水中加入规定剂量的液氯 液氯能够溶解于水 并且与水能够发生化学反应。近年来
| 传统的自来水处理剂是在自来水中加入规定剂量的液氯,液氯能够溶解于水,并且与水能够发生化学反应。近年来,科技工作者为了延长液氯的杀菌时间,在液氯中加入适量的液氨。 (1)请你写出液氯与水反应的化学方程式:____________________,氧化剂是______________,还原剂是 _____________。从氧化剂和还原剂来看,该反应的特点是______________,从元素化合价的变化来看,该反应的特点是______________。 (2)用液氯作为自来水的杀菌剂,起作用的是HClO,所以液氯加入水中后含氯的物质有氯单质、HClO和 ____________,其中氯单质可以从水中挥发,这正是我们有时打开自来水管能够闻到刺激性气味的原因,HClO也可以分解产生氧气和HCl。在液氯中加入少量液氨,生成NH2Cl,NH2Cl比HClO稳定。在HClO浓度大的时候发生的反应是NH3+HClO===H2O+NH2Cl,在HClO浓度小的时候发生的反应是H2O+NH2Cl==NH3↑+HClO,所以这种方法可以缓慢的放出HClO,起杀菌、消毒的作用,减少了氯的流失。以上两个反应的反应类型是________(填序号)。 A.氧化还原反应 B.非氧化还原反应 C.置换反应 D.复分解反应 |
参考解答
(1)H2O+Cl2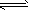 HCl+HClO;Cl2;Cl2;氧化剂和还原剂是同一种物质;同种元素的化合价既升高,又降低 HCl+HClO;Cl2;Cl2;氧化剂和还原剂是同一种物质;同种元素的化合价既升高,又降低 (2)HCl;BD |
相似问题
下列叙述正确的是 [ ]A.氧化还原反应的本质是化合价发生变化 B.有单质产生的分解反应
下列叙述正确的是 [ ]A.氧化还原反应的本质是化合价发生变化 B.有单质产生的分解反应一定是氧化还原反应 C.氧化剂在同一反应中既可以是反应
已知3Cu+8HNO3(稀) ===3Cu(NO3)2+2NO↑+4H2O 则下列说法不正确的是 [
已知3Cu+8HNO3(稀) ===3Cu(NO3)2+2NO↑+4H2O,则下列说法不正确的是 [ ]A.Cu作还原剂,HNO3作氧化剂 B.HNO3在该反应中只有部分表现出了氧化性 C.
某金属氧化物在光照下可生成具有很强氧化能力的物质 能用来消除空气或水体中的污染物。下列有关该金属氧化
某金属氧化物在光照下可生成具有很强氧化能力的物质,能用来消除空气或水体中的污染物。下列有关该金属氧化物的应用的叙述不正确的是 [ ]A.将形成酸雨
11P+ 15CuSO4+ 24H2O == 5Cu3P+ 6H3PO4 + 15H2SO4反应中
11P+ 15CuSO4+ 24H2O == 5Cu3P+ 6H3PO4 + 15H2SO4反应中,被氧化的P原子与被还原的P原子个数比是[ ]A.6:5 B.5:6 C.11:5 D.11:6
下列变化需要加入氧化剂才能实现的是 [ ]A. S2-→HS- B. HCO3-→CO2 C
下列变化需要加入氧化剂才能实现的是 [ ]A S2-→HS- B HCO3-→CO2 C 2I-→I2 D Cu2+→Cu












