如图是以食盐为原料进行生产并综合利用的某些过程.(1)为除去粗盐中的CaCl2 MgCl2和Na2S
如图是以食盐为原料进行生产并综合利用的某些过程.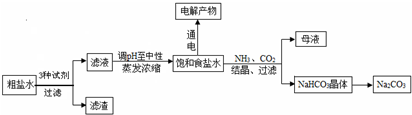 (1)为除去粗盐中的CaCl2、MgCl2和Na2SO4杂质,可对应加入过量的Na2CO3、过量的NaOH以及过量的BaCl2,其中Na2CO3必须在BaCl2之______(填“前”或“后”). (2)将滤液的pH调至中性应加入的试剂是______. (3)流程中所得饱和食盐水可用于制取纯碱等产品,其主要反应原理如下: NaCl+H2O+NH3+CO2=NaHCO3↓+NH4Cl2NaHCO3=Na2CO3+H2O+CO2↑ 问:分离出NaHCO3晶体后的母液中一定含有的溶质有______,若此母液中加入过量生石灰,则可获得一种可循环使用的物质,其化学式是______. (4)该流程的主要产品纯碱属于______(填“酸”或“碱”或“盐”). |
参考解答
| (1)总体思路是先沉淀再过滤,沉淀时要先加BaCl2溶液,再加Na2CO3溶液,因为碳酸钠能把过量的氯化钡沉淀出来,氢氧化钠可放在它们前面,也可放在它们后面或中间,都完全沉淀完后再过滤; (2)向滤液中加入适量的稀盐酸时,可以将滤液的pH调至中性,并且生成氯化钠不引入新的杂质; (3)由于NaCl+H2O+NH3+CO2=NaHCO3↓+NH4Cl,析出NaHCO3晶体并分离出后的母液一定是NaHCO3的饱和溶液,同时NH4Cl一定在溶液中.分离出NaHCO3晶体后的母液中含有氯化铵,加入过量生石灰后,氧化钙和水反应生成氢氧化钙,氢氧化钙和氯化铵反应能生成氯化钙、水和氨气,氨气可以循环使用,化学式是NH3. (4)Na2CO3由钠离子和碳酸钙离子组成,属于盐. 故答案为:(1)后 (2)稀盐酸 (3)NH4Cl、NaHCO3;NH3 (4)盐 |
相似问题
已知:A B C D E F六种物质是初中化学常见的物质。A B是单质 C D E都是氧化物。A B
已知:A、B、C、D、E、F六种物质是初中化学常见的物质。A、B是单质,C、D、E都是氧化物。A、B、C转化为F的过程较为复杂,F的成份也较复杂,其主要成分是
下图是初中化学中常见物质间的转化关系 其中C D G为单质 且G是目前世界年产量最高的金属 其余为化
下图是初中化学中常见物质间的转化关系,其中C、D、G为单质,且G是目前世界年产量最高的金属,其余为化合物。A是地球上最多的液态氧化物,F与H的组成元素
“NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl”是著名的”侯氏制碱法“的重要反应.下
“NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl”是著名的”侯氏制碱法“的重要反应.下面是4位同学对该反应涉及的有关知识发表的部分见解.其中不正确的是( )A
可生成二氧化碳的反应很多 例如:①酒精的燃烧②木炭在空气中燃烧③碳与氧化铜反应④高温煅烧石灰石⑤石灰
可生成二氧化碳的反应很多,例如:①酒精的燃烧②木炭在空气中燃烧③碳与氧化铜反应④高温煅烧石灰石⑤石灰石与稀硫酸反应⑥石灰石与稀盐酸反应⑦碳酸钙
下列四组转化关系中不能实现的一组是( )A.Na→Na20→NaOH→Na2CO3B.C→CO→C
下列四组转化关系中不能实现的一组是( )A.Na→Na20→NaOH→Na2CO3B.C→CO→CO2→H2CO3C.Fe203→Fe2(SO4)3→Fe(OH)3→FeCl3D.H2SO4→Na2SO4→NaNO3→AgNO3












