有一种工业废水 已知其中含有大量硫酸亚铁 少量硫酸铜和硫酸钠.今设计一种既经济又合理的方法 回收铜和
有一种工业废水,已知其中含有大量硫酸亚铁,少量硫酸铜和硫酸钠.今设计一种既经济又合理的方法,回收铜和硫酸亚铁.可使用的药品:铁、铜、稀硫酸、稀盐酸.设计方案与实验过程如图所示: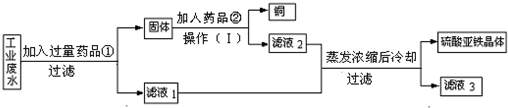 根据实验过程判断: (1)操作(Ⅰ)的名称是______. (2)写出加入药品①后发生的反应的化学方程式______. (3)加入药品②与操作(Ⅰ)的目的是______(用编号表示). a、分离出铜和增加滤液① b.除去过量的药品①和分离出铜 c.除去过量的药品①和增加滤液① (4)滤液3中,除溶质硫酸钠,还可能存在的溶质有______. |
参考解答
| (1)操作(Ⅰ)后得到了固体和滤液,可以知道该操作为过滤; (2)根据实验目的要收集铜和硫酸亚铁,所以应加入过量的铁来置换出铜,铁和硫酸铜反应生成了铜和硫酸亚铁,加入药品①后发生的反应的化学方程式为:Fe+CuSO4═Cu+FeSO4; (3)由于加入过量的铁,所以为了将铁转化为硫酸亚铁并分离出铜,应该加入稀硫酸来将多余的铁反应掉,同时可得到较纯的铜,故该实验目的为:b除去过量的药品①和分离出铜,故选b; (4)反应中加入的稀硫酸可能没完全反应,而硫酸亚铁也可能没全部结晶析出,所以滤液3中,除溶质硫酸钠,还可能存在的溶质有:FeSO4、H2SO4. 故答案为: (1)过滤; (2)Fe+CuSO4═Cu+FeSO4; (3)b; (4)FeSO4、H2SO4. |
相似问题
下列物质间的转化 不能通过一步反应实现的是( )A.Fe→FeCl2B.CuO→CuSO4C.CO
下列物质间的转化,不能通过一步反应实现的是( )A.Fe→FeCl2B.CuO→CuSO4C.CO→CO2D.C→CaCO3
许多科学家为人类进步作出了巨大贡献.发明“联合制碱法”的科学家是( )A.张青莲B.侯德榜C.拉瓦
许多科学家为人类进步作出了巨大贡献.发明“联合制碱法”的科学家是( )A.张青莲B.侯德榜C.拉瓦锡D.道尔顿
FeCl3广泛用于净水 制印刷电路等方面.下列各组物质能直接反应用来制取FeCl3的是( )A.F
FeCl3广泛用于净水、制印刷电路等方面.下列各组物质能直接反应用来制取FeCl3的是( )A.Fe与盐酸B.Fe2O3与盐酸C.BaCl2与FeSO4D.FeCO3与盐酸
下列变化 不能通过一步反应实现的是( )A.MgCl2→Mg(NO3)3B.Ba(OH)2→KOH
下列变化,不能通过一步反应实现的是( )A.MgCl2→Mg(NO3)3B.Ba(OH)2→KOHC.Cu→Cu(OH)2D.CaCl2→CaO
下列物质在玻璃 洗涤等工业上广泛应用 著名化学家侯德榜先生曾对改进它的生产技术做出过杰出贡献的是(
下列物质在玻璃、洗涤等工业上广泛应用,著名化学家侯德榜先生曾对改进它的生产技术做出过杰出贡献的是( )A.NaClB.Na2CO3C.CuSO4D.KNO3












