I.用元素符号回答原子序数11-18的元素的有关问题:(填对应物质的化学式)(1)最高价氧化物的水化
| I.用元素符号回答原子序数11-18的元素的有关问题:(填对应物质的化学式) (1)最高价氧化物的水化物碱性最强的是 ;其电子式为: (2)最高价氧化物的水化物呈两性的是 ; (3)能形成气态氢化物且最稳定的是 ,其电子式为 . II.化学是一门以实验为基础的自然科学,根据已有实验知识回答下列问题。 下列说法错误的是 。
F.实验室保存硫酸亚铁溶液,需在试剂瓶内加入铁粉或铁钉,防止硫酸亚铁被氧化 G.除去KCl溶液中少量MgCl2:加入适量NaOH溶液,过滤 |
参考解答
I.(1)NaOH,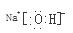 (2) Al(OH)3 (3)HCl, 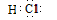 II.C E G |
试题分析:I.(1)原子序数11-18的元素中金属性最强的元素是Na,其最高价氧化物的水化物碱性最强,化学式为NaOH,电子式为 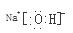 ; ;(2)原子序数11-18的元素中Al的最高价氧化物的水化物呈两性,是Al(OH)3 (3)原子序数11-18的元素中Cl元素的非金属性最强,气态氢化物最稳定,化学式为HCl,电子式为 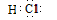 ; ;II.A、氯气溶于水显酸性,石蕊试液变红,同时有次氯酸生成,所以又褪色,正确;B、分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出,正确;C、托盘天秤称量固体时只能精确到0.1g,错误;D、常温下,铁与浓硫酸发生钝化,反应停止,正确;E、氯化铵分解产生氨气和氯化氢气体,遇冷又结合成氯化铵,得不到氨气,错误;F、硫酸亚铁空气中被氧化为硫酸铁,所以需在试剂瓶内加入铁粉或铁钉,防止硫酸亚铁被氧化,正确;G、除去KCl溶液中少量MgCl2:加入适量NaOH溶液,除去了镁离子,同时又增加了钠离子,错误,答案选C、E、G。 |
相似问题
X Y W M N五种元素分别位于周期表中三个紧邻的周期 且原子序数逐渐增大 X和Y的氢化物都比同族
X、Y、W、M、N五种元素分别位于周期表中三个紧邻的周期,且原子序数逐渐增大,X和Y的氢化物都比同族元素氢化物的沸点高,但在同周期中却不是最高的。W是
根据下表(部分短周期元素的原子半径及主要化合价)信息 判断以下叙述正确的是元素代号ABCDE原子半径
根据下表(部分短周期元素的原子半径及主要化合价)信息,判断以下叙述正确的是元素代号ABCDE原子半径 nm0 1860 1430 0890 1020 074主要化合价+1+3+2+6
短周期元素R T Q W G在元素周期表中的相对位置如图所示 其中Q是无机非金属材料的主角。下列判断
短周期元素R、T、Q、W、G在元素周期表中的相对位置如图所示,其中Q是无机非金属材料的主角。下列判断正确的是A.离子半径:T< W<GB.等物质的量的W、G单
已知X Y Z W四种元素是元素周期表中三个不同短周期的元素 且原子序数依次增大。X W同主族 Y
已知X、Y、Z、W四种元素是元素周期表中三个不同短周期的元素,且原子序数依次增大。X、W同主族,Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z原子最外
下表是元素周期表主族元素的一部分 短周期元素X的最高正化合价是+5 Y的单质可在空气中燃烧。WXY
下表是元素周期表主族元素的一部分,短周期元素X的最高正化合价是+5,Y的单质可在空气中燃烧。WXYZ请回答下列问题:(1)Z的元素符号是,写出Z的原子结构












