(8分)能源是人类生存和发展的重要支柱。研究化学反应过程中的能量变化在能源紧缺的今天具有重要的理论意
| (8分)能源是人类生存和发展的重要支柱。研究化学反应过程中的能量变化在能源紧缺的今天具有重要的理论意义。已知下列热化学方程式: ① 2H2(g)+O2(g)=2H2O(l) 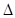 H=-570kJ/mol ;② H2(g)+1/2O2(g)=H2O(g) H=-570kJ/mol ;② H2(g)+1/2O2(g)=H2O(g) 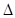 H="-242kJ/mol" H="-242kJ/mol" ③ C(s)+1/2O2(g)="CO" (g) 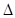 H=" —110.5kJ/moL" ④ C(s)+O2(g)=CO2(g) H=" —110.5kJ/moL" ④ C(s)+O2(g)=CO2(g) 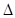 H="-393.5kJ/moL" H="-393.5kJ/moL" ⑤ CO2(g) +2H2O(g)=2CH4(g) +2 O2(g) 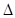 H=" +890kJ/moL" H=" +890kJ/moL" 回答下列问题: (1)上述反应中属于吸热反应的有(填写序号) 。 (2)H2的燃烧热为 。 (3)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然难直接测定,但可通过间接的方法求得。 已知C(s) + H2O(g) = H2(g)+ CO (g) 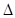 H=akJ/moL; H=akJ/moL;则a= ; 又已知自由能 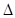 G= G=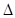 H—T H—T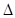 S,当 S,当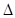 G<0时可自发进行。则该反应在什么条件下可自发进行 。 G<0时可自发进行。则该反应在什么条件下可自发进行 。 |
参考解答
| (1)⑤ (2)285KJ/mol或 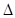 H=-285KJ/mol H=-285KJ/mol(3)+131.5 高温时 |
试题分析:吸热反应的表示方法是:ΔH>0 所以上述反应中属于吸热反应的只有⑤;H2的燃烧热为285KJ/mol;已知C(s) + H2O(g) = H2(g)+ CO (g) 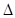 H=akJ/moL;由盖斯定律可得C(s) + H2O(g) = H2(g)+ CO (g) H=akJ/moL;由盖斯定律可得C(s) + H2O(g) = H2(g)+ CO (g) 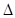 H=ΔH3—ΔH2=—110.5kJ/moL—(-242kJ/mol)=+131.5KJ/mol,所以a=+131.5 ;又已知自由能 H=ΔH3—ΔH2=—110.5kJ/moL—(-242kJ/mol)=+131.5KJ/mol,所以a=+131.5 ;又已知自由能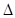 G= G=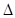 H—T H—T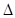 S,当 S,当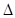 G<0时可自发进行。由热化学方程式可知:ΔH>0,ΔS>0,要保证ΔG<0则该反应在高温时条件下可自发进行。 G<0时可自发进行。由热化学方程式可知:ΔH>0,ΔS>0,要保证ΔG<0则该反应在高温时条件下可自发进行。点评:在25℃,101 kPa时,1 mol可燃物完全燃烧生成稳定的氧化物时所放出的热量,叫做该物质的燃烧热.单位为kJ/mol1。对于水来说,1mol可燃物完全燃烧必须生成液态水时放出的热量才能称为燃烧热,气态水不可以。) |
相似问题
某同学所做实验如图所示 向小试管中加入生石灰固体 充分反应后 U型管中a液面会下降 关于小试管内的化
某同学所做实验如图所示,向小试管中加入生石灰固体,充分反应后,U型管中a液面会下降,关于小试管内的化学反应说法正确的是①该反应为放热反应②生成物
下列说法正确的是 ( )A.π键是由两个p轨道“头碰头”重叠形成的B.σ键是镜像对称的 而π键是轴
下列说法正确的是 ( )A.π键是由两个p轨道“头碰头”重叠形成的B.σ键是镜像对称的,而π键是轴对称的C.乙烷分子中的键全为σ键,而乙烯分子中含
下列含有非极性键的离子化合物是A.CaCl2B.H2O2C.Na2O2D.CH4
下列含有非极性键的离子化合物是A.CaCl2B.H2O2C.Na2O2D.CH4
(8分)有下列八种晶体A.金刚石B.蔗糖C.氧化镁D.白磷 E.晶体氩F.铝 G.水晶 H 氢氧
(8分)有下列八种晶体A.金刚石B.蔗糖C.氧化镁D.白磷 E.晶体氩F.铝 G.水晶 H 氢氧化钠,用序号回答下列问题:(1)只有离子键构成的化合物是
(12分)(1)有下列物质:①冰②金刚石 ③碳化硅④干冰 ⑤过氧化氢 ⑥白磷 根据要求用序号填空。属
(12分)(1)有下列物质:①冰②金刚石③碳化硅④干冰⑤过氧化氢⑥白磷根据要求用序号填空。属于原子晶体的化合物是,由极性分子构成的晶体是,属于分子晶












