铝和氢氧化钾都是重要的工业产品。请回答(1)工业冶炼铝的化学方程式是________________
| 铝和氢氧化钾都是重要的工业产品。请回答 (1)工业冶炼铝的化学方程式是__________________________________。 (2)铝与氢氧化钾溶液反应的离子方程式是__________________________________。 (3)工业品氢氧化钾的溶液中含有某些含氧酸根杂质,可用离子交换膜法电解提纯。电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示。 |
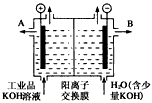 |
| ①该电解槽的阳极反应式是__________________________________。 ②通电开始后,阴极附近溶液pH会增大,请简述原因________________________________。 ③除去杂质后得氢氧化钾溶液从液体出口____________(填写A或B)导出。 |
参考解答
(1)2Al2O3 4Al+3O2↑ 4Al+3O2↑ (2)2Al+2H2O+2OH-==2AlO2-+3H2↑ (3)①4OH--4e-==O2↑+2H2O;②H+放电,促进水的电离,OH-浓度增大;③B |
相似问题
电解质量分数为0.052(5.2%)的NaOH溶液1 L(密度为1.06 g/cm3) 用铂作电极电
电解质量分数为0 052(5 2%)的NaOH溶液1 L(密度为1 06 g cm3),用铂作电极电解,当溶液中NaOH的质量分数改变了0 010(1 0%)时停止电解,此时溶液中符合下
用惰性电极电解下列溶液 一段时间后 再加入一定量的另一种物质(括号内物质) 电解液基本不变的是[
用惰性电极电解下列溶液,一段时间后,再加入一定量的另一种物质(括号内物质),电解液基本不变的是[ ]A.CuCl2(CuSO4) B.NaOH(NaOH) C.NaCl(HCl) D.CuSO4[Cu(OH)2]
用石墨作电极电解下列溶液 阳极上产生O2 阴极上产生H2的是[ ]A.HCl B.NaOHC
用石墨作电极电解下列溶液,阳极上产生O2,阴极上产生H2的是[ ]A.HCl B.NaOHC.CuSO4 D.KCl
下图是一种正在投入生产的大型蓄电系统的原理图。电池中的左右两侧为电极 中间为离子选择性膜 在电池放电
下图是一种正在投入生产的大型蓄电系统的原理图。电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜只允许钠离子通过。电池充、放电
如图所示 a b是多孔石墨电极 某同学按图示装置进行如下实验:断开K2 闭合K1一段时间 观察到两支
如图所示,a、b是多孔石墨电极,某同学按图示装置进行如下实验:断开K2,闭合K1一段时间,观察到两支玻璃管内都有气泡将电极包围,此时断开K1,闭合K2,












