(三选一)【化学—物质结构与性质】金属铜的导电性仅次于银 大量用于电气工业。(1)用金属键理论解释金
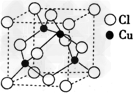
| (三选一)【化学—物质结构与性质】 金属铜的导电性仅次于银,大量用于电气工业。 (1)用金属键理论解释金属铜能导电的原因_______________。 (2)写出铜的基态原子核外电子排布式_______________。 (3)铜的某种氯化物晶体的晶胞结构如图所示,该氯化物的化学式为_______________。 |
 |
| (4)向硫酸铜溶液中加入过量氨水,然后加入适量乙醇,溶液中析出深蓝色的[Cu(NH3)4]SO4晶体。氨分子中N原子的杂化方式为____________ 。上述深蓝色晶体中含有的化学键除普通共价键外,还有_________和___________。 |
参考解答
| (1)金属铜晶体中的电子气在电场的作用下定向移动而导电 (2)1s22s22p63s23p63d104s1 (3)CuCl (4)sp3;离子键; 配位键 |
相似问题
氯化硼的熔点为-107℃ 沸点为12.5℃ 在其分子中键与键之间的夹角为120o 它能水解 有关叙述
氯化硼的熔点为-107℃,沸点为12 5℃,在其分子中键与键之间的夹角为120o,它能水解,有关叙述正确的是[ ]A.氯化硼液态时能导电而固态时不导电 B.硼
四种元素X Y Z W位于元素周期表的前四周期 已知它们的核电荷数依次增加 且核电荷数之和为51;Y
四种元素X、Y、Z、W位于元素周期表的前四周期,已知它们的核电荷数依次增加,且核电荷数之和为51;Y 原子的L层p轨道中有2个电子;Z与Y原子的价层电子数
果糖分子的结构简式为:CH2OH(CHOH)3COCH2OH 试写出其结构式。并用*标记出其中的手性
果糖分子的结构简式为:CH2OH(CHOH)3COCH2OH,试写出其结构式。并用*标记出其中的手性碳原子;在果糖分子中C原子以何种杂化轨道成键?成何种键? ______
碘单质在水溶液中溶解度很小 但在CCl4中溶解度很大 这是因为( )A.CCl4与I2分子量相差较
碘单质在水溶液中溶解度很小,但在CCl4中溶解度很大,这是因为( )A.CCl4与I2分子量相差较小,而H2O与I2分子量相差较大B.CCl4与I2都是直线型分子,
(三选一)【化学-物质结构与性质】乙炔是有机合成工业的一种原料。工业上曾用与水反应生成乙炔。(1)中
(三选一)【化学-物质结构与性质】乙炔是有机合成工业的一种原料。工业上曾用与水反应生成乙炔。(1)中互为等电子体,的电子式可表示为________;1mol中












