下表为元素周期表的一部分 请参照元素①-⑧在表中的位置 用化学用语回答下列问题(1)④ ⑤ ⑥的原子
| 下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题 |
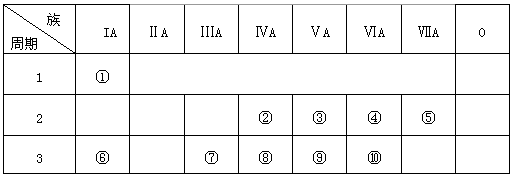 |
| (1)④、⑤、⑥的原子半径由大到小的顺序为_________________________。 (2)⑨、⑩的最高价含氧酸的酸性由强到弱的顺序是_________________________。 (3)①、④、⑥中的某些元素可形成既含离子键又含共价键的化合物,写出其中一种化合物的电子式:____________________。 (4)由表中④、⑩两种元素形成的氢化物中沸点高的是________,说明原因:____________________。 |
参考解答
| (1)Na>O>F (2)H2SO4>H3PO4 (3) 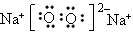 (或 (或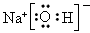 ) )(4)H2O;H2O分子间存在氢键 |
相似问题
下列有关原子结构和元素周期律表述正确的是[ ]①原子序数为15的元素的最高化合价为+3 ②Ⅶ
下列有关原子结构和元素周期律表述正确的是[ ]①原子序数为15的元素的最高化合价为+3 ②ⅦA族元素是同周期中非金属性最强的元素 ③第二周期ⅣA族元素
已知短周期元素的离子 aA2+ bB+ cC3- dD-都具有相同的电子层结构 则下列叙述正确的是
已知短周期元素的离子,aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是 [ ]A.原子半径A>B>C>DB.原子序数D>C>B>A C.离子半径C3->
W X Y是原子序数依次增大的同一短周期元素。W X是金属元素 它们的最高价氧化物的水化物之间可以反
W、X、Y是原子序数依次增大的同一短周期元素。W、X是金属元素,它们的最高价氧化物的水化物之间可以反应生成盐和水;Y的最外层电子数是核外电子层数的2倍
短周期金属元素甲~戊在元素周期表中的相对位置如下表所示 下列判断正确的是 [ ]A.原子半径
短周期金属元素甲~戊在元素周期表中的相对位置如下表所示,下列判断正确的是 [ ]A.原子半径:丙<丁<戊 B.金属性:甲>丙 C.氢氧化物碱性:丙>丁>戊
对Na Mg Al的有关性质的叙述正确的是[ ]A.碱性:NaOH<Mg(OH)2<Al(O
对Na、Mg、Al的有关性质的叙述正确的是[ ]A.碱性:NaOH<Mg(OH)2<Al(OH)3B.第一电离能:Na<Mg<AlC.电负性:Na>Mg>AlD.还原性:Na>Mg>Al












