(Ⅰ)溴乙烷在不同溶剂中与NaOH发生不同类型的反应 生成不同的反应产物。(1)写出溴乙烷在NaOH
| (Ⅰ)溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物。 (1)写出溴乙烷在NaOH水溶液中的反应方程式: 反应类型 。某同学取少量溴乙烷与NaOH水溶液反应后的混合溶液,向其中滴加AgNO3溶液,加热,产生少量沉淀。该同学由此得出溴乙烷与NaOH水溶液反应,生成了溴化钠,你认为是否合理,原因: 。 (2)写出溴乙烷在NaOH乙醇溶液中的反应方程式 反应类型 。反应中生成的气体可以用下图所示装置检验,现象是 ,水的作用是 。除高锰酸钾酸性溶液外,还可以用 检验生成的气体,此时还有必要将气体先通入水中吗? (填“有”或“没有”) 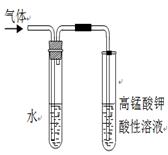 (Ⅱ)下面是实验室制乙烯并检验其性质的装置图,请回答: 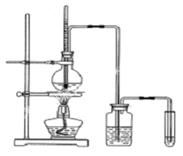 (1)写出圆底烧瓶中反应的方程式 , 反应类型_______________; (2)烧瓶中混合液逐渐变黑,并产生某些无机杂质气体,写出产生杂质气体的化学方程式: ; (3)为了检验乙烯的生成,试管中应盛放 , 现象为 ; (4)洗瓶中盛放的试剂为 ,作用________________________________。 (Ⅲ)某学习小组同学为了确定盐酸 、苯酚、碳酸的酸性强弱,设计了如图所示的装置图进行实验: 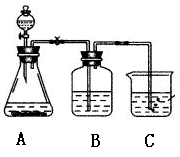 (1)锥形瓶内装某可溶性盐,写出A中反应的离子方程式: ; (2)C中的现象为 ,写出C中反应的化学方程式:_____________; (3)B中的试剂为 ,作用 。 |
参考解答
| (Ⅰ) (1)CH3CH2Br+NaOH→CH3CH2OH+NaBr 取代(或水解) 不合理 没有用硝酸中和氢氧化钠溶液 (2)CH3CH2Br+NaOH—→CH2=CH2↑+NaBr+H2O 消去反应 溶液褪色 吸收乙醇 溴的四氯化碳溶液 没有 (Ⅱ) (1)CH3CH2OH 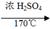 CH2=CH2↑ +H2O 消去反应 CH2=CH2↑ +H2O 消去反应(2) C + 2H2SO4(浓)  CO2↑ + 2SO2↑+ 2H2O CO2↑ + 2SO2↑+ 2H2O (3)高锰酸钾溶液(或溴的四氯化碳溶液) 溶液褪色 (4)氢氧化钠溶液 吸收SO2 CO2 (Ⅲ) (1)CO32-+ 2H+=H2O+ CO2↑ (2) 白色浑浊 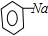 +CO2+H2O→ +CO2+H2O→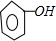 +NaHCO3 +NaHCO3(3)饱和碳酸氢钠溶液 吸收CO2中的HCl |
试题分析:(Ⅰ)(1)溴乙烷与NaOH水溶液发生水解反应(取代反应),反应方程式为CH3CH2Br+NaOH→CH3CH2OH+NaBr。由于AgNO3与NaOH溶液反应也生成沉淀,故不合理。 (2)溴乙烷与NaOH乙醇溶液发生消去反应,方程式为:CH3CH2Br+NaOH—→CH2=CH2↑+NaBr+H2O。高锰酸钾溶液能氧化乙烯气体而褪色。由于挥发出的乙醇也可被高锰酸钾溶液氧化,使高锰酸钾溶液褪色,应先除去,水的作用就是吸收乙醇。还可以用Br2与乙烯发生反应褪色来验证,其中不用先通入水中。 (Ⅲ)(2)二氧化碳、水和苯酚钠反应生成苯酚和碳酸氢钠,反应方程式为 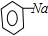 +CO2+H2O→ +CO2+H2O→ +NaHCO3。 +NaHCO3。点评:本题是有关实验方案的设计和评价的考查,要求学生熟悉所实验的内容及原理,能够考查同学们进行分析问题、解决问题的能力。 |
相似问题
能够鉴定溴乙烷中存在溴元素的实验操作是A.在溴乙烷中直接加入AgNO3溶液B.加入NaOH溶液 加热
能够鉴定溴乙烷中存在溴元素的实验操作是A.在溴乙烷中直接加入AgNO3溶液B.加入NaOH溶液,加热后加入稀硝酸酸化,然后加入AgNO3溶液C.加蒸馏水,充分搅
化学上通常把原子数和电子数相等的分子或离子称为等电子体 研究发现等电子体间结构和性质相似(等电子原理
化学上通常把原子数和电子数相等的分子或离子称为等电子体,研究发现等电子体间结构和性质相似(等电子原理)。化合物B3N3H6被称为无机苯,它与苯是等电
在光照条件下 将体积相同的甲烷气体和Cl2(常温 常压下)混和 得到物质的量最多的是:A.CH3Cl
在光照条件下,将体积相同的甲烷气体和Cl2(常温、常压下)混和,得到物质的量最多的是:A.CH3ClB.CH2Cl2C.CHCl3D.CCl4E.HCl
苯环结构中 不存在单双键交替结构 可以作为证据的事实是:①苯不能使酸性KMnO4溶液褪色;②苯环中碳
苯环结构中,不存在单双键交替结构,可以作为证据的事实是:①苯不能使酸性KMnO4溶液褪色;②苯环中碳碳键的键长均相等;③苯能在一定条件下跟H2发生加成
Ⅰ.下列实验操作不正确的是______;①用分液漏斗分离环己烷和苯的混合液体②将10滴溴乙烷加入到1
Ⅰ.下列实验操作不正确的是______;①用分液漏斗分离环己烷和苯的混合液体②将10滴溴乙烷加入到1mL10%的烧碱溶液中,加热片刻后,冷却,先加过量的硝酸












