(10分)硫酸工业中废渣称为硫酸渣 其成分为SiO2 Fe2O3 Al2O3 MgO。某探究性学习小
(10分)硫酸工业中废渣称为硫酸渣,其成分为SiO2、Fe2O3、Al2O3、MgO。某探究性学习小组的同学设计以下方案,进行硫酸渣中金属元素的提取实验。 已知:①Fe3+、Al3+和Mg2+以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、5.2和12.4;Al(OH)3完全溶解的pH为11.8。②常温下,饱和氨水的pH约为11。 已知:①Fe3+、Al3+和Mg2+以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、5.2和12.4;Al(OH)3完全溶解的pH为11.8。②常温下,饱和氨水的pH约为11。请回答:(1)写出A与氢氧化钠溶液反应的化学方程式: 。 (2)上述流程中试剂②应该是 (填以下字母编号)。
。 (4)计算溶液F中c(Mg2+)= ( 25℃时,氢氧化镁的Ksp=5.6×10-12)。 (5)工业生产中将固体C灼烧后的产物与KNO3、KOH固体加热共熔制备净水剂K2FeO4,同时获得一种亚硝酸盐,请写出制得K2FeO4的化学方程式: 。 |
参考解答
| (共10分,每空2分) (1)SiO2+2NaOH=Na2SiO3+H2O (反应物、产物写错0分;没配平,扣1分) (2)A(多选0分) (3)镁离子沉淀不完全及氢氧化铝溶解不完全(1个点1分) (4)5.6× 10–10 mol/L(单位1分) (5)Fe2O3+3KNO3+4KOH 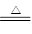 2K2FeO4+3KNO2+2H2O(物质写错0分;没配平、没条件扣1分) 2K2FeO4+3KNO2+2H2O(物质写错0分;没配平、没条件扣1分) |
试题分析:(1)混合物中和盐酸不反应的是二氧化硅,即固体A是二氧化硅。二氧化硅是酸性氧化物,则二氧化硅和氢氧化钠溶液反应的化学方程式是SiO2+2NaOH=Na2SiO3+H2O。 (2)溶液B中含有铁离子、铝离子和镁离子,所以根据氢氧化物沉淀时的pH可知,如果控制pH=3.7,析出的沉淀是氢氧化铁,即固体C是氢氧化铁。溶液B中含有铝离子和镁离子,则氢氧化物沉淀时的pH和氢氧化铝溶解时的pH可知,E时氢氧化镁,F是偏铝酸盐,所以试剂②是氢氧化钠,答案选A。 (3)如果pH过小,则会导致镁离子沉淀不完全及氢氧化铝溶解不完全,所以应该可知pH=13。 (4)由于溶液中OH-的浓度是0.1mol/L,所以根据氢氧化镁的溶度积常数可知,溶液中镁离子的浓度是 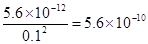 。 。(5)氢氧化铁分解生成氧化铁,所以根据原子守恒可知,制备高铁酸钾的化学方程式是Fe2O3+3KNO3+4KOH 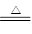 2K2FeO4+3KNO2+2H2O。 2K2FeO4+3KNO2+2H2O。点评:该题是高考中的常见题型,试题难度较大,对学生的要求高。本题关键是明确反应的原理,理解所给的信息,然后灵活运用即可。该题有利于学生的逻辑思维能力和灵活应变能力,有利于提高学生分析问题、解决问题的能力。该题综合性强,学生不易得分。 |
相似问题
下列分离提纯方法不正确的是A.除去酒精中的水 先加生石灰再用蒸馏法B.分离碘和氯化钠 用升华法C.分
下列分离提纯方法不正确的是A.除去酒精中的水,先加生石灰再用蒸馏法B.分离碘和氯化钠,用升华法C.分离四氯化碳和酸性高锰酸钾溶液,用分液法D.分离K
下列仪器常用于物质分离的是( )① ② ③ ④ ⑤ ⑥
下列仪器常用于物质分离的是()① ② ③ ④ ⑤⑥A.③⑤⑥ B.②③⑤ C.②④⑤ D.①②⑥
废旧电池进入环境后 对人体带来一系列的致畸 致癌 致变等危害。废电池中主要有铜帽(含Cu Zn) 锌
废旧电池进入环境后,对人体带来一系列的致畸、致癌、致变等危害。废电池中主要有铜帽(含Cu、Zn)、锌壳、铁片、石墨、填充物(MnO2、NH4Cl),对废旧电
锌和铝都是活泼金属 其氢氧化物均能既能溶于强酸 又能溶于强碱。但是氢氧化铝不溶于氨水 而氢氧化锌能溶
锌和铝都是活泼金属,其氢氧化物均能既能溶于强酸,又能溶于强碱。但是氢氧化铝不溶于氨水,而氢氧化锌能溶于氨水,生成配合物离子[Zn(NH3)4]2+。除去A
下列实验方案不合理的是A.用灼烧的方法区别人造丝和蚕丝 B.用水鉴别苯和乙醇C.实验室用N2和H2制
下列实验方案不合理的是A.用灼烧的方法区别人造丝和蚕丝 B.用水鉴别苯和乙醇C.实验室用N2和H2制备NH3D.用饱和NaHCO3溶液除去CO2中混有的SO2气体












