中和热的测定是高中重要的定量实验.取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫
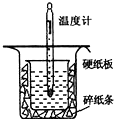
| 中和热的测定是高中重要的定量实验.取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸溶液50mL置于如图所示的装置中进行中和热的测定实验,回答下列问题: (1)从如图实验装置看,其中尚缺少的一种玻璃用品是______,除此之外,装置中的一个明显错误是______. (2)若改用60mL0.25mol?L-1H2SO4和50mL0.55mol?L-1NaOH溶液进行反应与上述实验相比,所放出的热量______(填“相等”“不相等”),若实验操作均正确,则所求中和热______填“相等”“不相等”). (3)实验数据如下表: ①请填写下表中的空白:
 | ||||||||||||||||||||||||||||||
参考解答
| (1)由量热计的构造可知该装置的缺少仪器是环形玻璃搅拌器;为了减少热量的损失,大烧杯杯口与小烧杯杯口相平; 故答案为:环形玻璃搅拌器;大烧杯杯口与小烧杯杯口没有相平; (2)反应放出的热量和所用酸以及碱的量的多少有关,并若用60mL0.25mol?L-1H2SO4溶液跟50mL0.55mol?L-1NaOH溶液进行反应,与上述实验相比,生成水的量增多,所放出的热量偏高,但是中和热的均是强酸和强碱反应生成1mol水时放出的热,中和热相等; 故答案为:不相等;相等; (3)①4次温度差分别为:3.4℃,6.1℃,3.3℃,3.5℃,第2组数据明显有误,所以删掉, 温度差平均值为
故答案为:3.4; ②0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸溶液50mL进行中和反应生成水的物质的量为0.05L×0.50mol=0.025mol,溶液的质量为:100ml×1g/ml=100g,温度变化的值△T为3.4℃来计算,则生成0.025mol水放出的热量为Q=m?c?△T=100g×4.18J/(g?℃)×3.4℃=1421.2J,即1.421kJ,所以实验测得的中和热△H=-
故答案为:-56.8 kJ/mol. |
相似问题
将V1 mL 1.0 mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶
将V1 mL 1 0 mol L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50 mL)。下列叙述
(1)CCl4和蒸馏水都是无色液体 请按下列要求用实验方法鉴别之(简要地写出实验过程) ① 只允许用
(1)CCl4和蒸馏水都是无色液体,请按下列要求用实验方法鉴别之(简要地写出实验过程) ① 只允许用一种试剂_________________________② 不用任何试
某研究小组成员在讨论鉴别浓硫酸和稀硫酸的方案时 设计如下标方案(1)其中可行的是__________
某研究小组成员在讨论鉴别浓硫酸和稀硫酸的方案时,设计如下标方案(1)其中可行的是____________(填序号)。(2)其中一个稍作改进就能成为可行的是_______
在生活 生产及化学研究中 人们经常需要根据不同原子 分子或离子的某些特征反应对物质进行检验 以确定物
在生活、生产及化学研究中,人们经常需要根据不同原子、分子或离子的某些特征反应对物质进行检验,以确定物质的组成。下列有关物质检验的说法止确的是[
关于焰色反应的叙述正确的是( )A.焰色反应是指可燃物在燃烧时所显示的火焰颜色B.灼烧氯化钡时火焰
关于焰色反应的叙述正确的是( )A.焰色反应是指可燃物在燃烧时所显示的火焰颜色B.灼烧氯化钡时火焰有特殊颜色C.做焰色反应实验结束后铂丝要用稀硫












