氯化汞(HgCl2)的凝固点降低常数为34.4 K.kg.mol-1。将0.849 g氯化亚汞(最简
氯化汞(HgCl2)的凝固点降低常数为34.4 K.kg.mol-1。将0.849 g氯化亚汞(最简式为HgCl)溶于50.0 gHgCl2中,所得混合物的凝固点降低了1.24℃,求氯化亚汞在该溶液中的摩尔质量及分子式。(相对原子质量:Hg 200,Cl35.5)
请帮忙给出正确答案和分析,谢谢!
参考解答
正确答案:难挥发、非电解质稀溶液凝固点降低公式:△Tf=Kf.b 设氯化亚汞在该溶液中的摩尔质量为M 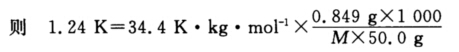 解得M=471 g.mol-1 HgCl的相对分子质量为235.5可见其分子式相当于两个最简式即为Hg2 Cl2。
解得M=471 g.mol-1 HgCl的相对分子质量为235.5可见其分子式相当于两个最简式即为Hg2 Cl2。
难挥发、非电解质稀溶液凝固点降低公式:△Tf=Kf.b设氯化亚汞在该溶液中的摩尔质量为M,解得M=471g.mol-1HgCl的相对分子质量为235.5,可见其分子式相当于两个最简式,即为Hg2Cl2。
相似问题
向0.030 mol.L-1的醋酸溶液中加入足量的固体醋酸钠 使溶液中醋酸钠的浓度为0.10 mol
向0.030 mol L-1的醋酸溶液中加入足量的固体醋酸钠,使溶液中醋酸钠的浓度为0.10 mol L-1(忽略固体加入后的体积变化)。已知醋酸的解离常数为1.8×10
某难挥发非电解质稀溶液的沸点为100.400℃ 则其凝固点为 ( )(水的Kb=0.512 K.kg
某难挥发非电解质稀溶液的沸点为100.400℃,则其凝固点为 ( )(水的Kb=0.512 K kg mol-1,Kf=1.86 K kg mol-1)A.一0.110℃B.一0.400℃C.一0.
采用电位滴定法 用0.20 mol.dm-3NaOH溶液滴定0.10 mol.dm-3HCl和0.1
采用电位滴定法,用0.20 mol dm-3NaOH溶液滴定0.10 mol dm-3HCl和0.10 mol dm-3H3PO4的混合溶液时,在电位滴定曲线上,可以出现2个突跃范围。 (
压力的改变对任何物质的溶解度都影响不大。 ( )此题为判断题(对 错)。请帮忙给出正确答案和分析 谢
压力的改变对任何物质的溶解度都影响不大。 ( )此题为判断题(对,错)。请帮忙给出正确答案和分析,谢谢!
进行下列计算:(已知Kaθ(HAc)=1.8×105) (1)0.10 mol.dm-3HAc的pH
进行下列计算:(已知Kaθ(HAc)=1.8×105) (1)0.10 mol dm-3HAc的pH,0.10 mol dm-3NaAc的pH各为多少? (2)将100 mL 0.10 mol dm-3HAc 与50 m












