锂电池消耗量巨大 对不可再生的金属资源的消耗是相当大的.因此锂离子电池回收具有重要意义 其中需要重点
锂电池消耗量巨大,对不可再生的金属资源的消耗是相当大的.因此锂离子电池回收具有重要意义,其中需要重点回收的是正极材料,其主要成分为钴酸锂(LiCoO2)、导电乙炔黑(一种炭黑)、铝箔以及有机粘接剂.某回收工艺流程如下: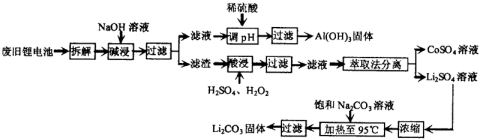 (1)上述工艺回收到的产物有Al(OH)3、______. (2)废旧电池可能由于放电不完全而残留有原子态的锂,为了安全,对拆解环境的要求是______. (3)酸浸时反应的化学方程式为______.如果用盐酸代替H2SO4和H2O2的混合液也能达到溶解的目的,但不利之处是______. (4)生成Li2CO3的化学反应方程式为______.已知Li2CO3在水中的溶解度随着温度的升高而减小,所以在浓缩结晶后要______过滤. |
参考解答
| (1)工艺流程的最终产物为:Al(OH)3、CoSO4、Li2CO3,故答案为:CoSO4、Li2CO3; (2)金属锂性质活泼,易与氧气、水发生反应,故答案为:隔绝空气和水分; (3)酸浸时反应物有硫酸、过氧化氢以及LiCoO2,生成物有Li2SO4和CoSO4,反应方程式为: 2LiCoO2+H2O2+3H2SO4=Li2SO4+2CoSO4+O2↑+4H2O,由题中信息知LiCoO2具有强氧化性,加入盐酸有污染性气体氯气生成, 故答案为:2LiCoO2+H2O2+3H2SO4=Li2SO4+2CoSO4+O2↑+4H2O;有氯气生成,污染较大; (4)碳酸锂难溶,生成Li2CO3的化学反应属于复分解反应,Li2CO3在水中的溶解度随着温度的升高而减小,应趁热过滤,故答案为:Li2SO4+Na2CO3=Na2SO4+Li2CO3↓;趁热. |
相似问题
下列反应中必须加入还原剂才能进行的是( )A.CuO→CuCl2B.Zn→Zn2+C.H2→H2O
下列反应中必须加入还原剂才能进行的是( )A.CuO→CuCl2B.Zn→Zn2+C.H2→H2OD.Fe3+→Fe2+
常温下 在溶液中可以发生反应:X+2Y3+=2Y2++X2+ 对下列叙述的判断正确的是( )①X被
常温下,在溶液中可以发生反应:X+2Y3+=2Y2++X2+,对下列叙述的判断正确的是( )①X被氧化②X是氧化剂③X具有还原性④Y2+是氧化产物⑤Y2+具有还原性
在反应Fe2O3+3CO═2Fe+3CO2中 ______是氧化剂;______元素被氧化 ____
在反应Fe2O3+3CO═2Fe+3CO2中,______是氧化剂;______元素被氧化,______元素被还原;四种物质中,______的还原性最强;在反应中每消耗1molCO就生成____
下列反应中不属于氧化还原反应的是( )A.Cl2+2NaOH═NaCl+NaClO+H2OB.NH
下列反应中不属于氧化还原反应的是( )A.Cl2+2NaOH═NaCl+NaClO+H2OB.NH3+HCl═NH4ClC.Br2+2KI═I2+2KBrD.2H2O2═2H2O+O2↑
某元素由化合态变为游离态 则该元素( )A.一定被氧化B.一定被还原C.可能被氧化可能被还原D.以
某元素由化合态变为游离态,则该元素( )A.一定被氧化B.一定被还原C.可能被氧化可能被还原D.以上都不是












