工业上可以用食盐和石灰石为原料制取纯碱(Na2CO3) 生产的关键是在沉淀池中让 NaCl NH3
工业上可以用食盐和石灰石为原料制取纯碱(Na2CO3),生产的关键是在沉淀池中让 NaCl、NH3、CO2和H2O尽可能多地转化成NaHCO3(固体沉淀物)和NH4Cl(溶液).主要生产流程如下: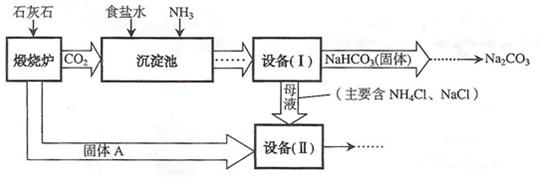 (已知2NH4CI+Ca(OH)2→CaCl2+2NH3↑+2H2O) (1)“煅烧炉”中发生反应的化学方程式是______. (2)若在化学实验室里分离“设备(I)”中的混合物,用到的操作名称是______. (3)在“设备(Ⅱ)”中固体A与水反应的化学方程式是______.该反应属于______反应(填写基本反应类型). (4)对“设备(Ⅱ)”中的母液处理后,除水以外可在本流程中再利用的物质有______(填写化学式). (5)请写出一个该生产流程的优点:______. |
参考解答
(1)碳酸钙在高温下分解生成二氧化碳气体和氧化钙,方程式为:CaCO3
(2)过滤是把不溶于溶液的固体和液体分开的一种分离混合物的方法,“设备(I)”中的液体混合物中分离出析出的晶体,可用过滤的方法. (3)氧化钙与水反应生成氢氧化钙,方程式为:H2O+CaO=Ca(OH)2,反应特点是“多变一”,符合化合反应的定义和特点. (4)进入“设备(Ⅱ)”的物质有氧化钙、氯化钠、氯化铵及水,发生的反应有H2O+CaO=Ca(OH)2、Ca(OH)2+2NH4Cl=2NH3↑+2H2O+CaCl2,最终产物有氯化钠、氯化钙、氨气,其中氯化钠、氨气可再利用. (5)从生产过程流程图可看出,使用的原料成本低、易得,且生产流程中有些物质可循环利用原料便宜易得(或者有物质可以循环利用) 故答案为:(1)CaCO3
(2)过滤; (3)H2O+CaO=Ca(OH)2;化合; (4)NH3、NaCl; (5)原料便宜易得(或者有物质可以循环利用). |
相似问题
某工厂的废水中只含氯化镁和少量盐酸 课外活动小组以此作为课题 探讨如何从中提取纯净的氯化镁固体.他们
某工厂的废水中只含氯化镁和少量盐酸,课外活动小组以此作为课题,探讨如何从中提取纯净的氯化镁固体.他们设计了两种不同的方案,请你参加讨论:(1)方
下列制取物质的设计中 不可能实现的是 [ ]A.CaCO3CaOCa(OH)2NaOH溶液B
下列制取物质的设计中,不可能实现的是 [ ]A.CaCO3CaOCa(OH)2NaOH溶液B.CuCuOCuSO4Cu(OH)2沉淀C.KMnO4O2SO3H2SO4D.Ba(OH)2BaCl2溶液BaCO3沉淀
制取硫酸铜有以下两种方法:第一种: Cu + 2H2SO4(浓) CuSO4 + SO2↑ + 2
制取硫酸铜有以下两种方法:第一种: Cu + 2H2SO4(浓) CuSO4 + SO2↑ + 2H2O;第二种:2Cu + O2 2CuO,CuO + H2SO4=CuSO4 +H2O。请回答
合乎实际并用于工业生产的是( )A.工业上用分离液态空气的方法制取氧气B.用工业酒精勾兑白酒C.高
合乎实际并用于工业生产的是( )A.工业上用分离液态空气的方法制取氧气B.用工业酒精勾兑白酒C.高温下用还原剂CO把Fe从它的氧化物中还原出来D.用Z
各物质间有着一定的反应关系和转化关系 下列各组物质间可以按下图所示关系直接转化的是( )A.Fe→
各物质间有着一定的反应关系和转化关系,下列各组物质间可以按下图所示关系直接转化的是( )A.Fe→Fe2O3→FeSO4→FeB.CO→CO2→H2CO3→COC.NaOH→












