Cu2S和稀HNO3反应生成Cu(NO3)2 H2SO4 NO和H2O 试解答下列各题(1)用双线桥
| Cu2S和稀HNO3反应生成Cu(NO3)2、H2SO4、NO和H2O,试解答下列各题 (1)用双线桥法标出电子转移的方向和数目 3Cu2S+22HNO3=6Cu(NO3)2+3H2SO4+10NO↑+8H2O (2)当产生0.1mol NO时,转移电子总数为_______,被还原的物质为_______mol,共耗HNO3_______ mol。 (3)被1mol Cu2S中+1价亚铜离子还原的HNO3的物质的量是_______mol |
参考解答
(1)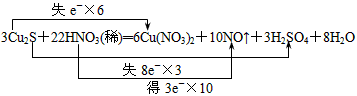 |
| (2)0.3×6.02×1023或1.806×1023;0.1;0.22 (3)2/3 |
相似问题
a mol FeS与b mol FeO投入到V L c mol·L-1的硝酸溶液中充分反应 产生NO
a mol FeS与b mol FeO投入到V L、c mol·L-1的硝酸溶液中充分反应,产生NO气体,所得澄清溶液成分可看作是Fe(NO3)3、H2SO4的混合液,则反应中未被
乙醇与重铬酸根离子在酸性溶液中能发生如下反应:C2H5OH+ Cr2O72- +H+→CO2↑+ C
乙醇与重铬酸根离子在酸性溶液中能发生如下反应:C2H5OH+ Cr2O72- +H+→CO2↑+ Cr3+ + H2O,当配平该反应方程式后,H+的化学计量数为 [ ]A.10 B.12 C.14D.16
写出符合下列条件的化学方程式(各举一例 并用单线桥法标出电子转移的方向和数目)。 (1)一种金属单质
写出符合下列条件的化学方程式(各举一例,并用单线桥法标出电子转移的方向和数目)。 (1)一种金属单质还原一种化合物;__; (2)一种单质氧化另一种单
对于反应2KMnO4+16HCl 2KCl+2MNCl2+5Cl2↑+8H2O 若有0.1molK
对于反应2KMnO4+16HCl2KCl+2MNCl2+5Cl2↑+8H2O,若有0 1molKMnO4参加反应,下列说法正确的是()A.还原剂是KMnO4B.生成Cl2 5 6LC.参加反应HCl为16molD.其转移电子0 5mol
亚硝酸钠(NaNO2)具有致癌作用 许多腌制食品中含NaNO2.酸性KMnO4溶液与亚硝酸钠发生的离
亚硝酸钠(NaNO2)具有致癌作用,许多腌制食品中含NaNO2.酸性KMnO4溶液与亚硝酸钠发生的离子反应为MnO4-+NO2-+H+-→Mn2++NO3-+H2O(未配平),下列叙述












