(15分)X Y Z W四种物质有如下相互转化关系(其中X W单质 Y Z为化合物 未列出反应条件)
(15分)X、Y、Z、W四种物质有如下相互转化关系(其中X、W单质,Y、Z为化合物,未列出反应条件)。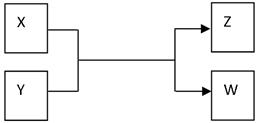 Ⅰ.若Z是生活中常用的调味品,W遇淀粉溶液变蓝,则: (1)常温下,X的颜色是 。 (2)工业上Z有多种用途,用化学方程式表示Z的一种用途 。 (3)生活中所用的Z加入了碘酸钾,过量X与Y溶液反应时可以得到一种碘酸盐,此反应的离子方程式是 。 Ⅱ.下面是某化学课外活动小组研究浓H2SO4的氧化性的结论并进行了实验验证: ①一般认为H2SO4浓度大于60%,就具有一定的强氧化性,越浓氧化性越强,60%以下的H2SO4主要体现的是酸性,基本上不体现强氧化性。 ②温度也影响氧化性,如铜放于冷的浓H2SO4中反应不明显,如果加热就可以观察到明显现象。 ③98%的浓H2SO4物质的量浓度为18.4 mol/L,密度为1.84 g·cm-3,根据以上信息回答: (1)如图装置,同学甲先向带支管的试管中放入铜粉和3 mL水,然后从分液漏斗中加98%的浓H2SO4 0.5 mL,加热至沸腾,该试管中液体没有明显变化,试用数据解释 原因 。 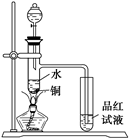 (2)乙同学利用所示装置直接从分液漏斗中再加浓H2SO4 10 mL与铜片反应。在左边试管中所观察到与甲不同的现象除了有黑色物质出现外,还有 ① , 原因是 。 ② , 原因是 。 |
参考解答
Ⅰ.(1)黄绿色 (1分) (2)2 NaCl +2 H2O  H2↑+ Cl2↑ + 2 NaOH (2分,答案合理均给分) H2↑+ Cl2↑ + 2 NaOH (2分,答案合理均给分)(3)3 Cl2 + I— + 3 H2O ='=' 6 Cl- + IO3— + 6 H+(2分) Ⅱ. (1)H2SO4溶液的质量分数为23%<60%,其氧化性不强,所以无明显现象。(2分) (2)①液体呈浅蓝色,(2分)溶液中含有Cu2+。(2分) ②有白色固体在试管底部析出,(2分) 98%浓H2SO4有吸水性,生成无水CuSO4。(2分) |
| 略 |
相似问题
放在敞口容器中的下列溶液 久置后溶液中溶质的浓度会变大的是()A.浓硫酸B.氢氧化钠C.浓盐酸D.氯
放在敞口容器中的下列溶液,久置后溶液中溶质的浓度会变大的是()A.浓硫酸B.氢氧化钠C.浓盐酸D.氯化钠
食盐中的加碘元素以KIO3形式存在。已知:IO-3+5I-+6H+====3I2+3H2O 根据此反
食盐中的加碘元素以KIO3形式存在。已知:IO-3+5I-+6H+====3I2+3H2O,根据此反应,可用试纸和一些生活中常见的物质进行检验,证明食盐中存在IO-3。可供选
铝 铁分别与足量的盐酸反应 若生成的气体在相同条件下体积相同 则铝和铁关系正确的是 ( )A.
铝、铁分别与足量的盐酸反应,若生成的气体在相同条件下体积相同,则铝和铁关系正确的是 ( )A.质量之比为9∶28B.物质的量之比为2∶3C.质量之比为28
漂粉精的有效成分是
漂粉精的有效成分是( )A.Ca(OH)2B.Ca(ClO)2 C.CaCl2D.CaCO3
关于酸 碱 盐的定义 下列各种说法中正确的是A.化合物电离出的阳离子有氢离子的就是酸B.化合物电离出
关于酸、碱、盐的定义,下列各种说法中正确的是A.化合物电离出的阳离子有氢离子的就是酸B.化合物电离出的阴离子有氢氧根离子的就是碱C.盐电离出的阳离












