利用下图装置采用适当试剂可完成实验某探究实验 并得出相应实验结论 实验所用试剂或所得结论列于表中.请
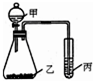
利用下图装置采用适当试剂可完成实验某探究实验,并得出相应实验结论,实验所用试剂或所得结论列于表中.请回答:
(2)请你根据上述实验装置再设计一个实验,并将选择的试剂、丙中的现象以及根据实验现象得出的实验结论填入下表.
 | ||||||||||||||||||||||||||
参考解答
| 解;(1)依据实验装置图可知,发生的反应为,甲和乙反应,生成产物通入丙中反应,如证明氧化性:KMnO4>Cl2>Br2,需要根据氧化还原反应的氧化剂的氧化性大于氧化产物的规律分析判断,甲为浓盐酸,滴入高锰酸钾溶液中生成氯气,氯气通入溴化钠溶液中会反应生成溴单质;高猛酸钾做氧化剂氧化盐酸中的氯化氢为氯气,氯气把氧化溴化钠中的溴离子为溴单质,符合氧化剂的氧化性大于氧化产物的规律应用,故答案为:浓盐酸,溴化钠溶液; (2)实验证明盐酸>碳酸,利用酸性强弱规律设计实验,元素和大理石反应生成二氧化碳气体,使澄清石灰水变浑浊;分液漏斗中的稀盐酸滴入盛大理石的锥形瓶中,反应生成二氧化碳气体,利用丙 装置检验二氧化碳的生成,证明盐酸酸性大于碳酸; 实验设计丙为石蕊试液,甲和乙试剂反应生成气体的性质验证,气体的性质需要是特征性质的验证,可以是验证氯气在石蕊试液中的现象是先变红,后褪色;甲为浓盐酸,乙为高锰酸钾溶液,反应生成的氯气通入石蕊试液后,氯气和水反应生成盐酸和次氯酸,具有酸性和漂白性;故答案为:  |
相似问题
根据下列反应判断有关物质的还原性由强到弱的顺序是[ ]H2SO3+I2+H2O=2HI+H2
根据下列反应判断有关物质的还原性由强到弱的顺序是[ ]H2SO3+I2+H2O=2HI+H2SO42FeCl3+2HI=2FeCl2+2HCl+I2 3FeCl2+4HNO3=2FeCl3+NO↑+2H2O+Fe(NO3)3 A
已知Cl- Fe2+ H2O2 I- SO2均具有还原性 且在酸性溶液中的还原性依次增强.下列各反应
已知Cl-、Fe2+、H2O2、I-、SO2均具有还原性,且在酸性溶液中的还原性依次增强.下列各反应不可能发生的是( )A.2Fe2++Cl2═2Fe3++2Cl-B.2Fe3+十SO2
R X Y和Z是四种常见的金属.已知XSO4与单质R不反应;XSO4+Z=X+ZSO4;Y+ZSO4
R、X、Y和Z是四种常见的金属.已知XSO4与单质R不反应;XSO4+Z=X+ZSO4;Y+ZSO4=YSO4+Z.四种金属的还原性顺序正确的是( )A.R>X>Y>ZB.X>R>Y>Z
在CuO和Fe粉混合物中 加入一定量稀硫酸微热 当反应停止后 滤出不溶物 并向滤液中插入一枚铁钉 发
在CuO和Fe粉混合物中,加入一定量稀硫酸微热,当反应停止后,滤出不溶物,并向滤液中插入一枚铁钉,发现铁钉并无任何变化.根据上述现象,确定下面结论正
下列反应既是氧化还原反应又是离子反应的是 [ ]A.钠在氯气中燃烧B.二氧化碳通入澄清的石灰
下列反应既是氧化还原反应又是离子反应的是 [ ]A.钠在氯气中燃烧B.二氧化碳通入澄清的石灰水中C.氯化钠溶液中滴加硝酸银溶液 D.锌粒放入稀硫酸中












