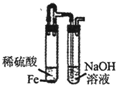
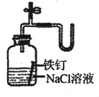
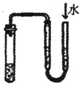
下列装置或操作不能达到实验目的是( )A.比较Cl2 Fe3+ I2的氧化性B.制取Fe(OH)2
下列装置或操作不能达到实验目的是( )
|
参考解答
| A、依据图中的操作,通入氯气会先和碘离子反应生成碘单质,然后再氧化亚铁离子生成三价铁离子,碘离子的还原性大于二价铁离子,说明三价铁离子的氧化性比碘单质强,可以比较氯气和Fe3+,氯气和I2的氧化性,故A能达到目的; B、装置中铁和稀硫酸反应生成了硫酸亚铁和氢气,由于氢氧化亚铁很易被空气中的氧气氧化看不到白色沉淀的生成,所以必须先排净试管内的空气,在使硫酸亚铁和氢氧化钠反应,装置中盛硫酸的试管中导气管为伸入溶液,硫酸亚铁无法压入后面的试管与氢氧化钠反应,所以达不到实验目的,故B不能达到目的; C、铁生锈要有空气和一定的湿度才行,在水里和盐溶液里面除了满足上述两个条件以外,还有加速铁生锈的另一个重要因素电解质,由于电解质的存在会大大加快生锈的速度,含量越高就越快,这也是在盐水里面生锈最快的原因.食盐水是电解质,电解质加速铁生锈的速度,根据右面红墨水液面的变化可证明铁生锈空气参与反应,故C能达到目的; D、检查装置气密性可以采取“注水法”:首先关闭排气导管,从顶部漏斗口注水,当漏斗下端被水封闭后再注水,水面不下降,表明装置气密性好;如果水面下降,表明装置气密性差,故D能达到目的; 故选B. |
相似问题
与铁相似 金属锡能溶于盐酸生成氯化亚锡 氯化亚锡又能被氯化铁氧化为氯化锡.则下列有关粒子氧化 还原能
与铁相似,金属锡能溶于盐酸生成氯化亚锡,氯化亚锡又能被氯化铁氧化为氯化锡.则下列有关粒子氧化、还原能力的比较中,正确的是 [ ]A.氧化能力:Sn4+
已知2FeCl3+2KI=2FeCl2+2KCl+I2 H2S+I2=2HI+S 下列叙述正确的是[
已知2FeCl3+2KI=2FeCl2+2KCl+I2,H2S+I2=2HI+S,下列叙述正确的是[ ]A、氧化性Fe3+>I2>SB、氧化性I2>S>Fe3+ C、还原性Fe2+>I->H2SD、还原性Fe2+>H2S>I-
下列说法可以实现的是 [ ]①酸性氧化物在一定条件下均能与碱发生反应
下列说法可以实现的是 [ ]①酸性氧化物在一定条件下均能与碱发生反应 ②弱酸与盐溶液反应可以生成强酸 ③发生复分解反应,但产物既没有水生成,也没
“二效催化转换器”可将汽车尾气中有毒气体处理为无污染的气体 下图为该反应的微观示意图(未配平) 其中
“二效催化转换器”可将汽车尾气中有毒气体处理为无污染的气体,下图为该反应的微观示意图(未配平),其中不同符号的球代表不同的原子。下列说法不正确的
已知I- Fe2+ SO2 Cl- 和H2O2均有还原性 它们在酸性溶液中还原性的顺序为SO2 >I
已知I-、Fe2+、SO2、Cl-、和H2O2均有还原性,它们在酸性溶液中还原性的顺序为SO2 >I->Fe2+ >H2O2>Cl-,则下列反应不可能发生的是 A、2Fe3+ + SO