2008年初我国南方遭遇的冰雪灾害中 使用了一种融雪剂 其主要成分的化学式为XY2 X原子的结构示意
2008年初我国南方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2,X原子的结构示意图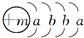 X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子. (1)m=______,该融雪剂的化学式为______. (2)Z、W元素的名称为______、______. (3)下列说法正确的是______. A.XY2和WZ2都为离子化合物 B.XY2分子中仅含离子键,WZ2中仅含极性共价键 C.H2Z比HY的稳定性强 D.X的阳离子比Y的阴离子半径大 (4)下列化学用语表达正确的是______. A.XY2的电子式: 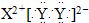 B.WZ2的结构式:Z=W=Z C.Y元素的单质与H2Z水溶液反应的离子方程式为:Y2+Z2-═2Y-+Z↓ D.用电子式表示XY2的形成过程为: 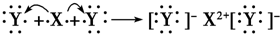 (5)冰雪的化学成分是H2O,水的沸点比H2Z的沸点高,其原因是______. |
参考解答
| (1)X为钙,Y为氯,所以m=20,融雪剂主要成分的化学式为CaCl2,故答案为:20;CaCl2; (2)因Z为硫,W为碳,故答案为:硫;碳; (3)A、因CS2是共价化合物,故A错误; B、因CaCl2中仅含离子键,CS2中只含共价键,且是极性共价键,故B正确; C、因氯的非金属性强于硫,所以稳定性HCl>H2S,故C错误; D、核外电子排布相同的离子,原子序数越小,离子的半径越大,所以半径Ca2+<Cl-; 故选:B. (4)A、CaCl2为离子化合物,电子式为: 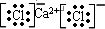 ,故A错误; B、CS2是直线形分子,结构式为S=C=S,故B正确; C、Cl2与H2S水溶液反应的离子方程式为:Cl2+H2S═2H++2Cl-+S↓,故C错误; D、CaCl2的形成过程为: 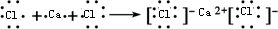 ,故D正确; 故选:BD. (5)因水分子中含有氢键,所以水的沸点比H2S的沸点高,故答案为:水分子中含有氢键. |
相似问题
下列化学 过程及其表述正确的是( )A.向NaHSO4溶液中滴入Ba(OH)2溶液呈中性:H++S
下列化学过程及其表述正确的是( )A.向NaHSO4溶液中滴入Ba(OH)2溶液呈中性:H++SO42-+Ba2++OH-═BaSO4↓+H2OB.由水电离的c(H+)=10-13mol?L-1的
向含有Fe3+ Cu2+ H+ NO -3的某稀溶液中逐渐加入Fe粉 Fe2+和Fe粉的物质的量关系
向含有Fe3+、Cu2+、H+、NO-3的某稀溶液中逐渐加入Fe粉,Fe2+和Fe粉的物质的量关系如图所示.则原稀溶液中Fe3+、Cu2+、H+的物质的量之比为( )A.1:2
下列离子方程式正确的是( )A.Cu2O溶于硝酸:Cu2O+2H+═2Cu++H2OB.向硅酸钠溶
下列离子方程式正确的是( )A.Cu2O溶于硝酸:Cu2O+2H+═2Cu++H2OB.向硅酸钠溶液中通人过量CO2:SiO32-+CO2+H2O═H2SiO3↓+CO32-C.硫酸氢铵溶液与
下列反应的离子方程式书写正确的是( )A.金属铝溶于氢氧化钠溶液Al+20H-=AlO2-+H2↑
下列反应的离子方程式书写正确的是( )A.金属铝溶于氢氧化钠溶液Al+20H-=AlO2-+H2↑B.钠和水反应Na+2H20=Na++20H-+H2↑C.金属铝溶于稀硫酸中:2Al
下列离子方程式正确的是( )A.向氯化亚铁溶液中通入氯气:Fe2++Cl2→Fe3++2Cl-B.
下列离子方程式正确的是( )A.向氯化亚铁溶液中通入氯气:Fe2++Cl2→Fe3++2Cl-B.用氢氧化钠溶液吸收少量二氧化碳:2OH-+CO2→CO32-+H2OC.向碳酸氢












