教材中给出了Na2O2与H2O反应的化学方程式2Na2O2+2H2O=4NaOH+O2↑。为了探究N
教材中给出了Na2O2与H2O反应的化学方程式2Na2O2+2H2O=4NaOH+O2↑。为了探究Na2O2与H2O反应的机理,某学习探究小组在教师指导下设计了如图所示装置进行实验。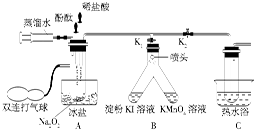 实验步骤如下: ①按图示组装仪器,并检查装置气密性为良好后装入药品。 ②保持K1打开、K2关闭,将注射器中的蒸馏水推入试管中,此时试管中并无气体产生。 ③挤压装有酚酞的胶头滴管,使酚酞滴入试管中,试管中溶液显红色。 ④挤压装有稀盐酸的胶头滴管,使稀盐酸滴入试管中,红色消失后再滴加2滴。 ⑤用双连打气球向A中试管中鼓气,使试管中溶液通过喷头进入B中支管中,发现淀粉-KI溶液变蓝,KMnO4溶液褪色。 ⑥迅速打开K2、关闭K1,继续向A中试管中鼓气,待试管中溶液进入C中试管中约三分之一时停止鼓气。然后用热水浴加热C中试管片刻,有气泡冒出,经检验为氧气。 请回答下列问题: (1)用离子方程式表示淀粉-KI溶液变蓝的原因:_____________________________ ________________________________________________________________________。 (2)用离子方程式表示KMnO4溶液褪色的原因: ______________________________ ________________________________________________________________________。 (3)A中用冰盐冷浴和C中用热水浴的作用分别是________、______________________。 (4)Na2O2与H2O反应的机理是____________________(用化学方程式表示)。 |
参考解答
| (1)2I-+2H++H2O2=I2+2H2O (2)2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O (3)防止生成的H2O2分解 使H2O2分解 (4)Na2O2+2H2O=2NaOH+H2O2,2H2O2  2H2O+O2↑ 2H2O+O2↑ |
| 开始试管中无气体生成,滴入酚酞,溶液变红色,说明Na2O2与H2O反应生成了碱和H2O2,然后滴入的稀盐酸中和NaOH,H2O2在C中分解生成O2。(1)H2O2有强氧化性能氧化I-。(2)H2O2使KMnO4溶液褪色,体现了其还原性。(3)A中用冰盐冷浴,防止温度过高H2O2分解,C中用热水浴可使H2O2分解。(4)Na2O2与H2O反应生成H2O2,H2O2遇热分解。 |
相似问题
下列叙述正确的是[ ]A.SO2具有还原性 故可作漂白剂 B.Na的金属活动性比Mg强 故可
下列叙述正确的是[ ]A.SO2具有还原性,故可作漂白剂 B.Na的金属活动性比Mg强,故可用Na与MgCl2溶液反应制MgC.浓硝酸中的HNO3见光会分解,故有时在实
对于实验Ⅰ~Ⅳ的实验现象预测正确的是A.实验Ⅰ:逐滴滴加盐酸时 试管中立即产生大量气泡B.实验Ⅱ:充
对于实验Ⅰ~Ⅳ的实验现象预测正确的是A.实验Ⅰ:逐滴滴加盐酸时,试管中立即产生大量气泡B.实验Ⅱ:充分振荡后静置,下层溶液为橙红色,上层无色C.实
有关苏打和小苏打的叙述正确的是A.苏打和小苏打都既能与酸反应又能与氢氧化钠反应B.与足量稀硫酸反应
有关苏打和小苏打的叙述正确的是A.苏打和小苏打都既能与酸反应又能与氢氧化钠反应B.与足量稀硫酸反应,生成等量的二氧化碳消耗的苏打的物质的量比小苏
向下列溶液中分别加入钠的小颗粒 溶液里无固体析出的是[ ]A.MgCl2溶液B.Ca(OH)
向下列溶液中分别加入钠的小颗粒,溶液里无固体析出的是[ ]A.MgCl2溶液B.Ca(OH)2饱和溶液C.CuSO4溶液 D.盐酸
关于钠元素 下列叙述中不正确的是[ ]A.钠离子与钠原子有相同的质子数 B.钠原子易失一 个
关于钠元素,下列叙述中不正确的是[ ]A.钠离子与钠原子有相同的质子数 B.钠原子易失一个电子,表现强氧化性 C.不同条件下,钠单质与氧气反应可生成












