某化工集团用氨碱法生产的纯碱中含有少量氯化钠杂质。为了测定该产品中碳酸钠的纯度 进行了以下实验:取1
某化工集团用氨碱法生产的纯碱中含有少量氯化钠杂质。为了测定该产品中碳酸钠的纯度,进行了以下实验:取16.5 g纯碱样品放入烧杯中,将烧杯放在电子天平上,再把150.0 g稀盐酸(足量)加入样品中。观察读数变化如下表所示:
(1)实验中产生的CO2气体质量为 ; (2)该产品中碳酸钠的质量分数 (结果精确到小数点后一位) 。 |
参考解答
| (1) 6.6克 [2分,未写单位扣1分 (2) 96.4% [3分 |
试题分析:(1)根据比值数据可知,反应进行到10s时,气体的物质的量不再发生变化,所以CO2的质量是208.6g-215.2g=6.6g。 (2)根据碳原子守恒可知,碳酸钠的质量是 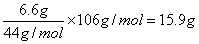 ,则该产品中碳酸钠的质量分数是 ,则该产品中碳酸钠的质量分数是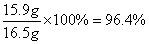 点评:该题是高考中的常见题型和考点,属于基础性试题的考查,侧重对学生基础知识的巩固和训练,有利于培养学生的逻辑推理能力和规范答题能力,提高学生灵活运用基础知识解决实际问题的能力。 |
相似问题
下列关于Na2O和Na2O2的叙述正确的是A.都是白色固体B.都能和水反应形成强碱溶液 C.都是碱性
下列关于Na2O和Na2O2的叙述正确的是A.都是白色固体B.都能和水反应形成强碱溶液 C.都是碱性氧化物D.都是强氧化剂
关于Na2CO3和NaHCO3性质的有关叙述正确的是( )A.在水中的溶解性:Na2CO3
关于Na2CO3和NaHCO3性质的有关叙述正确的是( )A.在水中的溶解性:Na2CO3<NaHCO3B.热稳定性:Na2CO3<NaHCO3C.与酸反应的快慢:Na2CO3<NaHCO3D.Na2C
美国“海狼”潜艇上的核反应堆内使用了液体铝钠合金(单质钠和单质铝熔合而成)作载热介质 有关说法不正确
美国“海狼”潜艇上的核反应堆内使用了液体铝钠合金(单质钠和单质铝熔合而成)作载热介质,有关说法不正确的是A.原子半径:r(Na)>r(Al)B.铝钠合金若
一块表面被氧化的钠质量是8.5g 投入到水中 完全反应得到标准状况下的H2 0.1g 则原钠块中被氧
一块表面被氧化的钠质量是8 5g,投入到水中,完全反应得到标准状况下的H20 1g,则原钠块中被氧化的钠的质量是A.2 3gB.4 6gC.6 2gD.7 8g
(11分)为证明有关物质的性质 某学生设计了如图所示的装置。当打开活塞C 使液体A与隔板H上的固体B
(11分)为证明有关物质的性质,某学生设计了如图所示的装置。当打开活塞C,使液体A与隔板H上的固体B相遇时,即有气体产生,并发现D中蜡烛熄灭;关闭C 打












