(10分)欲用含有少量氯化钙的氯化钠固体 配制100 mL 1mol/L的氯化钠溶液 设计了下面的操
(10分)欲用含有少量氯化钙的氯化钠固体,配制100 mL 1mol/L的氯化钠溶液,设计了下面的操作方案。根据方案操作步骤回答下列问题: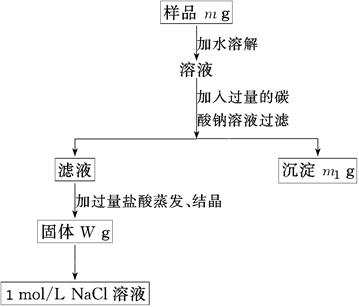 ⑴称量粗盐样品m g,样品放在托盘天平左盘上。 ⑵过滤时,需用到的玻璃仪器除烧杯、玻璃棒外有 。 ⑶蒸发操作时应将液体放在___ ___中加热,等加热至____ ____时即停止加热。 ⑷在样品的溶液中加入过量的Na2CO3溶液,作用是____________________________,反应的离子方程式是___ ___________________。 ⑸在滤液中加入盐酸的作用是________ ________,发生反应的化学方程式是____ _______。 ⑹配制100 mL 1mol/L的NaCl溶液时,应从W g固体中称取NaCl的质量为____________。 |
参考解答
| (10分,每空1分,方程式各2分) (2)漏斗 (3)蒸发皿 剩余较少液体 (4)使钙离子完全形成沉淀而除去 Ca2++CO32—-===CaCO3↓ (5)除去过量的Na2CO3 Na2CO3+2HCl===2NaCl+H2O+CO2↑ (6)5.9 g |
试题分析:(2)过滤时,需用到的玻璃仪器除烧杯、玻璃棒外有漏斗。 (3)蒸发操作时应将液体放在蒸发皿中加热,等加热至剩余较少液体时即停止加热。 (4)氯化钠中含有氯化钙,所以在样品的溶液中加入过量的Na2CO3溶液的作用是使钙离子完全形成沉淀而除去,反应的离子方程式是Ca2++CO32—-===CaCO3↓。 (5)由于碳酸钠是过量的,所以在滤液中加入盐酸的作用是除去过量的Na2CO3,有关反应的化学方程式是Na2CO3+2HCl===2NaCl+H2O+CO2↑。 (6)100 mL 1mol/L的NaCl溶液只溶质的质量是0.1L×0.1mol/L×58.5g/mol=5.85g。由于托盘天平只能读数到0.1g,所以实际称量的质量是5.9g。 点评:化学实验常用仪器的使用方法和化学实验基本操作是进行化学实验的基础,对化学实验的考查离不开化学实验的基本操作,所以本部分内容主要是以常见仪器的选用、实验基本操作为中心,通过是什么、为什么和怎样做重点考查实验基本操作的规范性和准确及灵活运用知识解决实际问题的能力。 |
相似问题
为了除去铁粉中的少量铝粉 可以选取下列哪种溶液 ( )A.浓盐酸B.浓硝酸C.浓硫酸D.浓氢氧
为了除去铁粉中的少量铝粉,可以选取下列哪种溶液( )A.浓盐酸B.浓硝酸C.浓硫酸D.浓氢氧化钠溶液
下列除去杂质的方法正确的是 ①除去乙烷中少量的乙烯:一定条件下
下列除去杂质的方法正确的是①除去乙烷中少量的乙烯:一定条件下通入H2 ②除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤,分液、干燥、蒸馏 ③获得
痕检是公安机关提取犯罪嫌疑人指纹的一种重要的方法 AgNO3显现法就是其中的一种:人的手上有汗渍 用
痕检是公安机关提取犯罪嫌疑人指纹的一种重要的方法,AgNO3显现法就是其中的一种:人的手上有汗渍,用手动过白纸后,手指纹线就留在纸上。如果将溶液①小
下列各组物质 能用一种试剂鉴别的是( )A.苯 己烯 甲苯B.乙酸 乙醛 乙醇C.乙醛 溴乙烷
下列各组物质,能用一种试剂鉴别的是()A.苯、己烯、甲苯B.乙酸、乙醛、乙醇C.乙醛、溴乙烷、硝基苯D.苯酚、乙醇、甘油
现有①乙酸乙酯和碳酸钠溶液;②甲醇和乙醇;③溴化钠和溴水三组混合物 分离它们的正确方法依次是A.分液
现有①乙酸乙酯和碳酸钠溶液;②甲醇和乙醇;③溴化钠和溴水三组混合物,分离它们的正确方法依次是A.分液萃取蒸馏B.萃取蒸馏分液C.分液蒸馏萃取D.蒸












