(Ⅰ)(4分)自然界里氮的固定途径之一是在闪电的作用下 N2与O2反应生成NO。(1)反应需要在闪电
| (Ⅰ)(4分)自然界里氮的固定途径之一是在闪电的作用下,N2与O2反应生成NO。 (1)反应需要在闪电或极高温条件下发生,说明该反应_________。(填字母) A.所需的活化能很高 B.吸收的能量很多 (2)在不同温度下,反应N2(g)+O2(g) 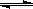 2NO(g)的平衡常数K如下表: 2NO(g)的平衡常数K如下表:
(3)2404℃时,在容积为1.0L的密闭容器中通入2.6mol N2和2.6mol O2,计算反应N2(g)+O2(g) 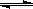 2NO(g)达到平衡时NO的浓度为 。(此温度下不考虑O2与NO的反应。计算结果保留两位有效数字) 2NO(g)达到平衡时NO的浓度为 。(此温度下不考虑O2与NO的反应。计算结果保留两位有效数字)(Ⅱ)(5分)在容积为1L的密闭容器中,进行如下反应:A(g)+2B(g) 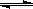 C(g)+D(g),不同温度下,D的物质的量n(D)和时间t的关系如图。试回答下列问题: C(g)+D(g),不同温度下,D的物质的量n(D)和时间t的关系如图。试回答下列问题: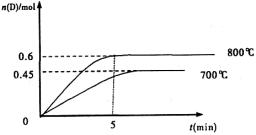 (1)能判断该反应达到化学平衡状态的依据是 。 A.容器中压强不变 B.混合气体中c(A)不变 C.2v正(B)=v逆(D) D.c(A)=c(C) (2)若最初加入1.0molA和2.2molB,利用图中数据计算800℃时的平衡常数K= ,该反应为 反应(填吸热或放热) (3)700℃时,某时刻测得体系中各物质的量如下:n(A)=1.1mol,n(B)=2.6mol,n(C)=0.9mol,n(D)=0.9mol,则此时该反应 进行(填“向正反应方向”“向逆反应方向”或“处于平衡状态”)。 |
参考解答
| (1)A(1分) (2)>(1分) (3)设NO的平衡浓度为x N2(g) + O2(g) 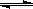 2NO(g) 2NO(g)起始时各物质浓度/ mol·L-1: 2.6 2.6 0 平衡时各物质浓度/ mol·L-1 2.6-x/2 2.6-x/2 x  x=0.20 mol·L-1(2分) (Ⅱ)(1)AB(2分,漏一个扣1分,错选不得分) (2)0.9(mol·L—1)—1(单位可不写) 吸热(2分) (3)向正反应方向(1分) |
| (1)氮气分子内的氮氮三键,键能极大,导致反应的活化能特别高,需要外界提供足够的能量才能发生化学反应; (2)升高温度,K值增大,平衡右移,说明正反应为吸热反应,△H>0 (3)设NO的平衡浓度为x N2(g) + O2(g) 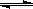 2NO(g) 2NO(g)起始时各物质浓度/ mol·L-1: 2.6 2.6 0 平衡时各物质浓度/ mol·L-1 2.6-x/2 2.6-x/2 x  x=0.20 mol·L-1(2分) (Ⅱ)(1)在恒容条件下: A.该可逆反应的两边的气体系数不等,故气体的总物质的量为变量,容器内的压强也是变量,当不变时,说明已达到平衡状态,正确 B.混合气体中c(A)不变,则各物质浓度均将不变,符合平衡状态的特征,正确 C.以不同物质的来表示正逆反应速率时,两速率数值上应符合系数比才能表示达到平衡,排除 D.不能说明任何问题,排除 答案为AB (2)反应:A(g)+2B(g) 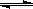 C(g)+D(g) C(g)+D(g)初n: 1.0 2.2 0 0 △n: 0.6 1.2 0.6 0.6 平衡n: 0.4 1.0 0.6 0.6 800℃时的平衡常数K=  =0.9(mol·L—1)—1 =0.9(mol·L—1)—1由图示可知,升温时,D的量增大,平衡右移,正反应为吸热反应; (3)依据所给数据可求得700℃时K=0.28,而此时刻的  =0.11,故反应将向正反应方向移动。 =0.11,故反应将向正反应方向移动。 |
相似问题
恒压密闭容器中充入2molX和5molY 发生反应: 温度分别为T1和T2时 X的转化率随时间变化的
恒压密闭容器中充入2molX和5molY,发生反应:,温度分别为T1和T2时,X的转化率随时间变化的关系如右图所示。则下列结论正确的是A.达到平衡后,其它条件不变
(10分)痛风是关节炎反复发作及产生肾结石为特征的一类疾病 关节炎的原因归结于在关节滑液中形成了尿酸
(10分)痛风是关节炎反复发作及产生肾结石为特征的一类疾病,关节炎的原因归结于在关节滑液中形成了尿酸钠(NaUr)晶体,有关平衡如下:①HUr(尿酸,aq)Ur-
在容积相等的两个密闭容器A和B中 保持温度为423K 同时向A B中分别加入a mol和b mol
在容积相等的两个密闭容器A和B中,保持温度为423K,同时向A、B中分别加入a mol和b mol HI(a > b),发生反应2HI(g) H2(g)+I2(g)达到平衡后,下列说
.对于可逆反应C(s)+H2O(g) CO(g)+H2(g) ΔH>0 达到平衡 下列说法正确的是
对于可逆反应C(s)+H2O(g) CO(g)+H2(g) ,ΔH>0,达到平衡,下列说法正确的是( )A.升高温度,平衡向逆反应方向移动B.加入固体碳,平衡向正反应方向移
在一定条件下 在容积为2L的密闭容器中 将2 mol 气体M和3 mol N气体混合 发生如下反应:
在一定条件下,在容积为2L的密闭容器中,将2 mol 气体M和3 mol N气体混合,发生如下反应:2M(g) + 3N(g) x Q(g) +3R(g),该反应达平衡时,生成2












