一定条件下的密闭容器中:4NH3(g)+5O2(g)4NO(g)+6H2O(g)+3623KJ;下列
一定条件下的密闭容器中:4NH3(g)+5O2(g) 4NO(g)+6H2O(g)+3623KJ;下列叙述正确的是 4NO(g)+6H2O(g)+3623KJ;下列叙述正确的是
|
参考解答
| C |
分析:A、根据热化学反应方程式中的热量变化来分析化学平衡中的热量; B、利用同一物质的v正=v逆来判断化学反应是否达到化学平衡; C、根据压强对化学平衡的影响及M= 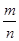 来分析; 来分析;D、根据温度对化学平衡的影响来分析. 解:A、因热化学反应方程式中的热量是物质完全转化时的能量变化,而在密闭容器中充入4molNH3与足量氧气充分反应不会完全转化,则放出的热量小于3623KJ,故A错误; B、由方程式可知,v正(O2)= 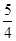 v正(NO),则v正(O2)= v正(NO),则v正(O2)=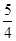 v逆(NO)时v正(NO)=v逆(NO)反应达到化学平衡,故B错误; v逆(NO)时v正(NO)=v逆(NO)反应达到化学平衡,故B错误;C、对于该反应,降低压强,化学平衡正向移动,由M= 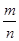 ,m不变,n变大,则M变小,即混合气体平均摩尔质量减小,故C正确; ,m不变,n变大,则M变小,即混合气体平均摩尔质量减小,故C正确;D、因该反应为放热反应,则升高温度,化学平衡逆向移动,混合气体中NO含量减小,故D错误; 故选C. |
相似问题
当一个可逆反应进行到正反应速率与逆反应速率相等的时候 就达到了“化学平衡”。下列关于化学平衡的说法中
当一个可逆反应进行到正反应速率与逆反应速率相等的时候,就达到了“化学平衡”。下列关于化学平衡的说法中正确的是①可逆反应达到化学平衡时,反应物与
(6分)在一个容积不变的反应容器中 可以通过调节温度使下列反应:A(g)+2B(g)2C(g) 达到
(6分)在一个容积不变的反应容器中,可以通过调节温度使下列反应:A(g)+2B(g)2C(g) 达到平衡时保持容器内气体的总物质的量为15 mol。现向反应容器中
下列四个图像的有关描述正确的是注:E:表示能量 p1>p2表示压强 t表示时间 V表示体积 B%表示
下列四个图像的有关描述正确的是注:E:表示能量,p1>p2表示压强,t表示时间,V表示体积,B%表示B的体积百分含量。A 图①表示化学反应的能量变化,该反应的
现有3个体积相等的密闭容器。都进行下列反应:CO2(g)+H2(g) H2O(g)+CO(g) 反应
现有3个体积相等的密闭容器。都进行下列反应:CO2(g)+H2(g)H2O(g)+CO(g),反应所处的温度相同,但起始浓度不同。其中甲:CO2 = H2 =" a" mol;乙
(7分)某温度时 在2 L的密闭容器中 X Y Z三种物质的量随时间的变化曲线如图所示。①由图中所给
(7分)某温度时,在2 L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示。①由图中所给数据进行分析,该反应的化学方程式为;②反应从开始












