(20分)己知:(1)2C(石墨s)+O2 (g) =' 2' CO(g) △H=-222KJ/
(20分)己知: (1)2C(石墨s)+O2  (g) =" 2" CO(g) △H=-222KJ/mol (g) =" 2" CO(g) △H=-222KJ/mol(2)2 H2(g)+O2(g)="2" H2O(g) △H=-484KJ/mol (3)C(石墨s)+O2(g)=CO2(g) △H=-393.5KJ/mo  l l(4)H2O(g)=H2O(L) △H=-44KJ/mol (5)C(金刚石s)+O2(g)=CO2(g) △H=-395.4KJ/mol 回答下列问题: (1)C(石墨)的燃烧热为 。 (2)写出表示H2的燃烧热的热化学方程式:  。 。(3)写出石墨转化为金刚石的热化学方程式(可不注明条件) 。相对更稳定的物质是 。 (4)工业上制H2的一个重要反应是:CO(g)+H2O(g)CO2 (g)+H2(g) ①该反应的△H= 。 ②为了提高CO的转化率,下列措施可采用的是 。
④800℃时,该反应的平衡常数K=1,则850℃时K 1(填.>、<、=) ⑤800℃时,若起始浓度:C(CO)="1" mol/L, C(H2O)=4mol/L,则达平衡时,C(H2)= ,CO的转化率为 。 |
参考解答
| (20分) (1)393.5KJ/mol (2)H2(g)+ 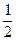 O2(g)=H2O(L) △H=-286KJ/mol O2(g)=H2O(L) △H=-286KJ/mol(3)C(石墨s)=C(金刚石s) △H='+1.9KJ/mol ' 石墨 (4)①-40.5KJ/mol ②D ③K= 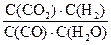 ④<1 ⑤0.8mol/L, 80% ④<1 ⑤0.8mol/L, 80% |
| 略 |
相似问题
在一定温度下 将1 mol N2和3 mol H2放入恒容密闭容器中 达到平衡时 测得NH3为0.8
在一定温度下,将1 mol N2和3 mol H2放入恒容密闭容器中,达到平衡时,测得NH3为0 8 mol,如果此时再加入1 mol N2和3 mol H2,达到新平衡时,NH
(14分)反应aA(g)+bB(g)cC(g)(H<0)在等容条件下进行。改变其他反应条件 在I I
(14分)反应aA(g)+bB(g)cC(g)(H<0)在等容条件下进行。改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如下图所示:回答
对于达到平衡的反应:2A(g)+B(g) nC(g) 符合右图所示的结论是A.P1>P2 n>3B
对于达到平衡的反应:2A(g)+B(g) nC(g),符合右图所示的结论是A.P1>P2,n>3B.P1>P2,n<3 C.P1<P2, n>3D.P1<P2, n<3
吸热反应N2(g)+O2(g)2NO(g) 在2000℃时 K=6.2×10-4。2000℃时 在1
吸热反应N2(g)+O2(g)2NO(g),在2000℃时,K=6 2×10-4。2000℃时,在10L密闭容器内放入2 94×10-3mol NO、2 50×10-1mol N2和4 00×10-2mo
下列对于反应C(s)+H2O(g)CO(g)+H2(g)的描述正确的是A.达到平衡时 各反应物和生成
下列对于反应C(s)+H2O(g)CO(g)+H2(g)的描述正确的是A.达到平衡时,各反应物和生成物浓度相同B.增大压强,对此反应速率无影响C.达到平衡时,c












