石灰石的主要成分是碳酸钙(其中杂质不参加任何反应) 某厂家为了测定当地矿山石灰石中碳酸钙含量以确定价
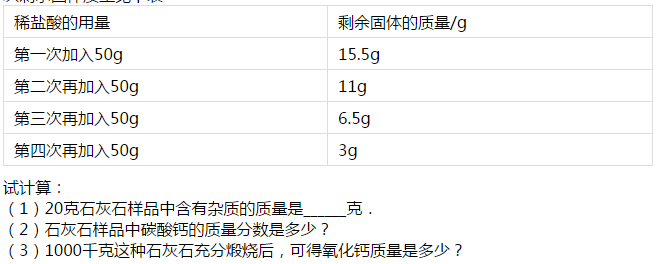
石灰石的主要成分是碳酸钙(其中杂质不参加任何反应),某厂家为了测定当地矿山石灰石中碳酸钙含量以确定价格.他们取样20克,并把200克稀盐酸分四次加入,充分反应后,每次剩余固体质量见下表
参考解答
| (1)由表格数据可知,每加入50g盐酸会消耗4.5g固体,分析知第四次加入时碳酸钙已无剩余,故固体中的杂质质量是3g; (2)石灰石样品中碳酸钙的质量分数是:
(3)设1000千克这种石灰石充分煅烧后,可得氧化钙质量是X CaCO3
100 56 1000Kg×85% X
答:(1)20克石灰石样品中含有杂质的质量是3克;(2)石灰石样品中碳酸钙的质量分数是85%;(3)1000千克这种石灰石充分煅烧后,可得氧化钙质量是476kg. |
相似问题
甲厂排出的废水每吨含氨(NH3)10.2g 乙厂排出的废水每吨含甲醇(CH3OH)8g.某污水处理厂
甲厂排出的废水每吨含氨(NH3)10 2g,乙厂排出的废水每吨含甲醇(CH3OH)8g.某污水处理厂利用现代先进的生化技术巧妙地将这两种污水混合,在某种细菌的
测定大理石含CaCO3的质量分数 取大理石12.5g 加入盛有100g稀盐酸的烧杯中 两者恰好完全反
测定大理石含CaCO3的质量分数,取大理石12 5g,加入盛有100g稀盐酸的烧杯中,两者恰好完全反应(假设其他杂质不与盐酸反应,也不溶解).烧杯内物质的质
今有镁 锌两种金属混合物7.7g 与足量的稀盐酸充分反应 产生的气体能使12g氧化铜恰好被还原 求原
今有镁、锌两种金属混合物7 7g,与足量的稀盐酸充分反应,产生的气体能使12g氧化铜恰好被还原,求原混合物中镁、锌各自的质量.
已知化学反应:2A+B=2C+4D 当10g A和8g B刚好完全反应后 生成6g C.则A B C
已知化学反应:2A+B=2C+4D,当10gA和8gB刚好完全反应后,生成6gC.则A、B、C、D的相对分子质量比是( )A.10:8:6:12B.5:4:3:6C.5:8:3:3D.2:1:2:4
常温下 把碳酸钠和氯化钠组成的固体混合物18.9g放人烧杯中 然后加入50g水 不断搅拌至全部溶解
常温下,把碳酸钠和氯化钠组成的固体混合物18 9g放人烧杯中,然后加入50g水,不断搅拌至全部溶解,制成溶液.往其中逐渐滴加溶质质量分数为10%的稀盐酸,












