有盐酸和氯化铜的混合溶液共100g 向该溶液中逐滴加入质量分数为10%的氢氧化钠溶液 生成的沉淀与加
有盐酸和氯化铜的混合溶液共100g,向该溶液中逐滴加入质量分数为10%的氢氧化钠溶液,生成的沉淀与加入的10%的氢氧化钠溶液的质量关系如如图所示.若氯化铜在原混合溶液中的质量分数为13.5%.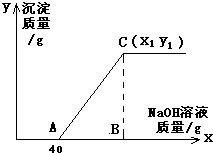 求:(1)原混合溶液中HCl的质量分数; (2)C点的坐标(x1、y1)为多少? |
参考解答
| (1)由关系图可知,与混合溶液中盐酸发生反应的氢氧化钠溶液的质量为40g,其中氢氧化钠的质量=40g×10%=4g; 设反应消耗HCl的质量为x NaOH+HCl═NaCl+H2O 40 36.5 4g x
原混合溶液中HCl的质量分数=
(2)混合溶液中含氯化铜的质量=100g×13.5%=13.5g 设反应消耗氢氧化钠的质量为y,反应生成沉淀氢氧化铜的质量为y1 CuCl2+2NaOH═Cu(OH)2↓+2NaCl 135 80 98 13.5g y y1
整个过程所消耗氢氧化钠溶液的总质量x1=40g+8g÷10%=120g 答:(1)原混合溶液中HCl的质量分数为3.65%;(2)C点的坐标为(120,9.8). |
相似问题
某中学化学课外活动小组的同学在实验室测定一批生理盐水中NaCl的质量分数.取该生理盐水130克 向其
某中学化学课外活动小组的同学在实验室测定一批生理盐水中NaCl的质量分数.取该生理盐水130克,向其中加入足量的AgN03溶液完全反应后,生成氯化银沉淀2 8
取等质量的氢氧化钠和碳酸钠固体 分别加入同一溶质质量分数的盐酸 恰好完全反应后溶质均为NaCl.若与
取等质量的氢氧化钠和碳酸钠固体,分别加入同一溶质质量分数的盐酸,恰好完全反应后溶质均为NaCl.若与氢氧化钠反应用去盐酸ag,与碳酸钠反应用去盐酸bg
在一密闭的真空容器内高温加热CuO和C的混合物.充分反应后 容器内的物质为金属单质和一种纯净的气体
在一密闭的真空容器内高温加热CuO和C的混合物.充分反应后,容器内的物质为金属单质和一种纯净的气体,则混合物中CuO和C的质量比可能是( )A.40:3B
工业上高温煅烧石灰石可形成生石灰和二氧化碳.高温锻烧150t含碳酸钙80%的石灰石 最多可制得氧化钙
工业上高温煅烧石灰石可形成生石灰和二氧化碳.高温锻烧150t含碳酸钙80%的石灰石,最多可制得氧化钙多少吨?
用32.5克锌与足量的稀硫酸反应 生成氢气的质量是多少克?在标准状况下的体积是多少升?(标准状况下氢
用32 5克锌与足量的稀硫酸反应,生成氢气的质量是多少克?在标准状况下的体积是多少升?(标准状况下氢气的密度:0 09克 升)












