称取铜 锌混合物粉末10.0g置于烧杯中 慢慢加入稀硫酸使其充分反应 直至固体质量不再减少为止 此时
| 称取铜、锌混合物粉末10.0g置于烧杯中,慢慢加入稀硫酸使其充分反应,直至固体质量不再减少为止,此时用去49.0g稀硫酸,剩余固体3.5g。 (1)该混合物粉末中铜的质量分数为多少? (2)所用的稀硫酸溶质的质量分数是多少? |
参考解答
(1)铜的质量分数=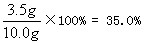 (2)设所用稀硫酸溶质的质量分数为x Zn+H2SO4==ZnSO4+H2↑ 65 98 10.0g-3.5g 49g×x 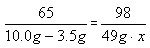 x= 20.0% |
相似问题
把等体积 等质量分数的稀硫酸放入两个烧杯中 将两烧杯放在天平的两个托盘上调平 再同时分别加入相同质量
把等体积、等质量分数的稀硫酸放入两个烧杯中,将两烧杯放在天平的两个托盘上调平,再同时分别加入相同质量的锌粒和铁粒,则可能观察到的现象是[ ]A.天
现将25.3g含有少量KNO3杂质的Na2CO3粉末样品 置于锥形瓶中加适量水配制成溶液 向其中逐滴
现将25 3g含有少量KNO3杂质的Na2CO3粉末样品,置于锥形瓶中加适量水配制成溶液,向其中逐滴加入未知溶质质量分数的CaCl2溶液直至过量,过程中锥形瓶里溶
Cu 20g与硫酸反应的化学方程式为Cu2O+H2SO4=Cu+CuSO4+H2O。氧化铜与氢气反应
Cu 20g与硫酸反应的化学方程式为Cu2O+H2SO4=Cu+CuSO4+H2O。氧化铜与氢气反应后得到的Cu中常常混有少量Cu2O。现将10 g Cu和Cu2O的混合物放入足量的稀硫
配制50g溶质的质量分数为4%的氢氧化钠溶液 需要氢氧化钠和水各多少克?若要完全中和这些溶液 需要溶
配制50g溶质的质量分数为4%的氢氧化钠溶液,需要氢氧化钠和水各多少克?若要完全中和这些溶液,需要溶质的质量分数为3 65%的稀盐酸多少克?
在我国推广使用“清洁燃料”的过程中 2005年5月16日上海交通大学宣布:我国首台使用二甲醚为燃料的
在我国推广使用“清洁燃料”的过程中,2005年5月16日上海交通大学宣布:我国首台使用二甲醚为燃料的城市客车问世,这将有效地解决公交车冒黑烟的问题。(












