(1)课外活动小组对空气中氧气含量的测定做了如下实验:在由两个注射器组成的密闭系统内有50mL空气
| (1)课外活动小组对空气中氧气含量的测定做了如下实验:在由两个注射器组成的密闭系统内有50mL空气,如图.然后给装有铜丝的玻璃管加热.同时交替推动两个注射器活塞,至玻璃管内铜丝变黑且较长时间内无进一步变化时停止.停止加热后,待冷却至室温将气体全部推至一个注射器内. ①验结束后,注射器内空气的体积减少了约______mL,这是因为______ ②在实验的加热过程中,交替缓慢推动两个注射器的目的是______. ③上述实验只是粗略测定空气中氧气含量的一种方法,你认为造成该实验不够精确的可能原因是______. (2)课外活动小组发现红热的铜丝变黑后,为了回收再利用铜丝,在研究如何除去黑色物质的讨论中,制定了下列方案. 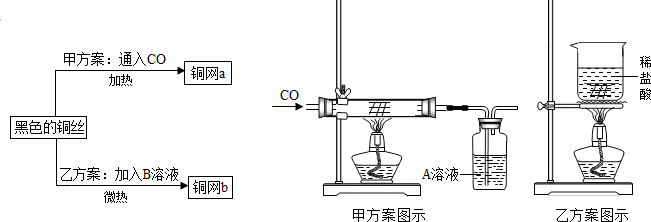 ①乙方案的烧杯中发生反应的化学方程式为______. 两种方案相比,______方案更好,其原因是______ ②若采用甲、乙两种方案处理此变成黑色的铜丝,并且充分反应,则回收的铜丝a的质量______(填“<”、“>”、“=”)铜丝b的质量.请通过分析和计算,采用甲、乙两种方案分别回收铜丝,所得到铜丝的质量理论上最多相差多少克?(提示:假设该实验中所取空气中氧气的密度为1.30g/L.要求:计算结果精确到0.01g.) 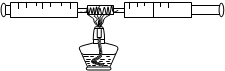 |
参考解答
(1)由于铜的氧化反应只消耗掉了空气中的氧气,而氧气在空气中约占空气体积的
(2)①碱性氧化物与酸反应生成盐和水可写出化学方程式:CuO+2HCl=CuCl2+H2O;从实验操作与环境保护方面看用乙方案要好些,故答案为:乙;甲方案使用CO,操作不便,浪费能源,而且可能对环境造成污染 ②两种方案一种是用一氧化碳还原氧化铜,另一种是用盐酸去除表面的氧化铜,从两种方案的反应原理可知铜丝a的质量要大于铜丝b的质量. 实验消耗氧气的质量:0.01L×1.3g/L=0.013g 设被0.013g氧气氧化的铜的质量为x 2Cu+O2
2×64 32 x 0.013g
x=0.05g,这0.05g铜最终进入了溶液,所以b最后剩余的铜就少了0.05g 答案为:a铜丝质量>b铜丝质量,理论上a铜丝比b铜丝多0.05g |
相似问题
在汞 食盐 明矾 干冰 钛合金五种物质中 生活中常用作调味剂的是______;可用于人工降雨的是__
在汞、食盐、明矾、干冰、钛合金五种物质中,生活中常用作调味剂的是______;可用于人工降雨的是______;能用来作净水剂的是______;体温计里的银白色金
在①纯碱 ②汞 ③食盐 ④熟石灰 ⑤干冰 ⑥烧碱 ⑦酒精七种物质中 生活中常用作调味剂的是_____
在①纯碱、②汞、③食盐、④熟石灰、⑤干冰、⑥烧碱、⑦酒精七种物质中,生活中常用作调味剂的是______;可用于人工降雨的是______;能用来改良酸性土壤
“粗盐提纯”的实验中 蒸发时 下列操作正确的是( )A.把还浑浊的滤液倒入蒸发皿里加热蒸发B.开始
“粗盐提纯”的实验中,蒸发时,下列操作正确的是( )A.把还浑浊的滤液倒入蒸发皿里加热蒸发B.开始析出晶体后,要用玻璃棒不断搅拌液体C.蒸发皿中
下列说法不正确的是( )A.某化肥与碱共热 若产生能使无色酚酞溶液变红的气体 则证明是铵态氮肥B.
下列说法不正确的是( )A.某化肥与碱共热,若产生能使无色酚酞溶液变红的气体,则证明是铵态氮肥B.木炭还原氧化铜实验中能观察到黑色粉末中有红色
通过海水晒制可得粗盐 粗盐除NaCl外 还含有MgCl2 CaCl2 MgSO4以及泥沙等杂质.以下
通过海水晒制可得粗盐,粗盐除NaCl外,还含有MgCl2、CaCl2、MgSO4以及泥沙等杂质.以下是制备精盐的实验方案:回答下列问题:(1)操作1中,加入NaOH溶液












