(6分)浓硫酸是重要的化工原料。试回答:(1)一个硫酸分子(H2SO4)中含有 个原
| (6分)浓硫酸是重要的化工原料。试回答: (1)一个硫酸分子(H2SO4)中含有 个原子。 (2)硫酸中氢、硫、氧三种元素的质量比为 。 (3)稀硫酸与其它酸都具有相似的性质是因为酸中都含有 。 (4)配制200g 24.5% 的稀硫酸需 98%的浓硫酸 g。 (5)为测定某氢氧化钠溶液的溶质质量分数,取25g该氢氧化钠溶液,滴加3—4滴酚酞,然后逐滴滴加上述24.5%的稀硫酸,待溶液由无色恰好变成无色时,测得共用去稀硫酸10g,则该氢氧化钠溶液的溶质质量分数为 。(写出计算过程)(2分) |
参考解答
| (1)7(2)2:32:64 (或1:16:32)(3)H+(或氢离子)(4)50 g;(5)8% |
试题分析: 解:(1)由H2SO4可知一个硫酸分子(H2SO4)中含有的7个原子; (2)由H2SO4可知硫酸中氢、硫、氧三种元素的质量比=(1×2):(32×1):(16×4)=1:16:32; (3)稀硫酸与其它酸都具有相似的性质是因为酸中都含有氢离子(H+); (4)设需98%的浓硫酸的质量为x。 200g×24.5%=98%·x x=50g 答:需98%的浓硫酸的质量为50g。 (5)设25g该氢氧化钠溶液中氢氧化钠的质量为y。 H2SO4 +2NaOH═Na2SO4+2H2O 98 80 10g×24.5% y 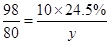 y=2g 该氢氧化钠溶液的溶质质量分数= 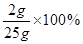 =8% =8%答:该氢氧化钠溶液的溶质质量分数为8%。 故答案为:(1)7(2)2:32:64 (或1:16:32)(3)H+(或氢离子)(4)50 g;(5)8% 点评:本题主要考查学生利用化学方程式进行计算的能力;解题的关键是正确运用化学方程式;计算时要注意格式。 |
相似问题
以下是根据一些反应事实推导出的影响化学反应的因素 其中不合理的是序号化学反应事实影响化学反应的因素A
以下是根据一些反应事实推导出的影响化学反应的因素,其中不合理的是序号化学反应事实影响化学反应的因素A铁丝在空气中很难燃烧,而在氧气中能剧烈燃烧反
(6分)根据所学知识回答下列问题:A B C
(6分)根据所学知识回答下列问题:A B C D E(1)实验室用高锰酸钾制取氧气的化学方程式是,所选用的发生装置是(填字母),用C装置收集氧气后,验满
(20分)实验室常用下列装置制取气体 请你根据所学知识回答下列问题。(1)写出编号所指仪器的名称:①
(20分)实验室常用下列装置制取气体,请你根据所学知识回答下列问题。(1)写出编号所指仪器的名称:①;②。(2)以上装置图中共有两处明显的错误,请
下列关于氧气的物理性质的叙述中 不正确的是( )A.氧气不易溶于水B.氧气的密度比空气略大C.液态
下列关于氧气的物理性质的叙述中,不正确的是( )A.氧气不易溶于水B.氧气的密度比空气略大C.液态氧是没有颜色的D.通常状况下氧气是一种无色无味的气体
下列物质在氧气中燃烧 生成黑色固体的是A.红磷B.铁丝C.木炭D.氢气
下列物质在氧气中燃烧,生成黑色固体的是A.红磷B.铁丝C.木炭D.氢气












