Mn Fe均为第四周期过渡元素 两元素的部分电离能(I)数据列于下表:元素MnFe电离能/kJ?mo
Mn、Fe均为第四周期过渡元素,两元素的部分电离能(I)数据列于下表:
(1)Mn元素价电子层的电子排布式为______,比较两元素的I2、I3可知,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难.对此,你的解释是______. (2)Fe原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物,则与Fe原子或离子形成配合物的分子或离子应具备的条件是______. (3)三氯化铁常温下为固体,熔点282℃,沸点315℃,在300℃以上易升华,易溶于水,也易溶于乙醚、丙酮等有机溶剂,据此判断三氯化铁晶体为______晶体. (4)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示.面心立方晶胞和体心立方晶胞中实际含有的Fe原子个数之比为______,其中体心立方晶胞空间利用率为______. 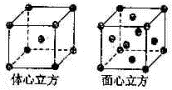 | ||||||||||||||
参考解答
| (1)Mn元素为25号元素,核外电子排布式为[Ar3d54s2,所以价层电子排布式为3d54s2, 由Mn2+转化为Mn3+时,3d能级由较稳定的3d5半充满状态转为不稳定的3d4状态需要的能量较多;而Fe2+到Fe3+时,3d能级由不稳定的3d6到稳定的3d5半充满状态,需要的能量相对要少, 故答案为:3d54s2;由Mn2+转化为Mn3+时,3d能级由较稳定的3d5半充满状态转为不稳定的3d4状态需要的能量较多;而Fe2+到Fe3+时,3d能级由不稳定的3d6到稳定的3d5半充满状态,需要的能量相对要少; (2)Fe原子或离子含有空轨道.所以,与Fe原子或离子形成配合物的分子或离子应具有孤对电子,故答案为:具有孤对电子; (3)三氯化铁,其熔点:282℃,沸点315℃,在300℃以上升华.易溶于水,也易溶于乙醚、丙酮等有机溶剂.符号分子晶体的特征,故为三氯化铁分子晶体, 故答案为:分子; (4)面心立方结构晶胞中铁原子数为1+6×
故答案为:2:1;68%. |
相似问题
下列对化学知识概括合理的是( )。A.原子晶体 离子晶体 金属晶体 分子晶体中都一定存在化学键B.
下列对化学知识概括合理的是()。A.原子晶体、离子晶体、金属晶体、分子晶体中都一定存在化学键B.同素异形体之间的转化都是物理变化C.原子晶体的熔点
下列说法中正确的是[ ]A.离子化合物中一定不含共价键 共价化合物中一定不含离子键 B.水分
下列说法中正确的是[ ]A.离子化合物中一定不含共价键,共价化合物中一定不含离子键 B.水分子呈直线形,氨分子呈三角锥形 C.碳原子之间可形成碳碳单
某化学学习兴趣小组 为了研究晶体的结构和性质 查阅了一水合硫酸四氨合铜(Ⅱ)([Cu(NH3)4]S
某化学学习兴趣小组,为了研究晶体的结构和性质,查阅了一水合硫酸四氨合铜(Ⅱ)([Cu(NH3)4]SO4)-H2O相关资料:一水合硫酸四氨合铜(Ⅱ)([Cu(NH3
用价层电子对互斥理论预测SO2和NO3-的立体结构 两个结论都正确的是 [ ]A.直线形;
用价层电子对互斥理论预测SO2和NO3-的立体结构,两个结论都正确的是 [ ]A.直线形;三角锥形 B.V形;三角锥形 C.直线形;平面三角形 D.V形;平面三角形
下列各组微粒的化学式中能真实表示分子组成的是( )A.NaClB.SiO2 C.SiD.P4
下列各组微粒的化学式中能真实表示分子组成的是()A.NaClB.SiO2 C.SiD.P4












