(11分)某合金由A B C D 四种元素组成 这四种元素位于周期表中前四周期 A是主要成分元素 A
| (11分)某合金由A、B、C、D 四种元素组成,这四种元素位于周期表中前四周期,A是主要成分元素,A的基态原子中有4个未成对电子。B是第一主要的合金元素,B的含量不低于11%,否则不能生成致密氧化膜BO3防止腐蚀,B与A同周期,且原子核外未成对电子数最多。C位于周期表中第4行、第10列,D的基态原子的最外层电子数是其电子层数的2倍,未成对电子数与电子层数相等。 (1)A的原子结构示意图是 。A的一种晶体的晶胞如图甲,乙图中●和○表示的是同种原子,即乙是8个甲无隙并置的结果,若按甲图中虚线方向切乙,得到a~d图中正确的是 。 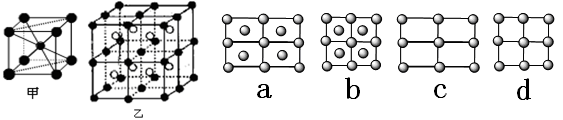 (2)写出B原子的基态的外围电子排布式_________________,与B同周期且基态原子最外层电子数与B相同的元素,可能位于周期表中的___区和 ___区。 (3)基态D原子的外围电子排布图是 。据报道,只含镁、C和D三种元素的晶体竟然具有超导性。该晶体的结构(如图示)可看作由镁原子和C原子在一起进行面心立方密堆积,该晶体的化学式为 。晶体中每个  原子周围距离最近的 原子周围距离最近的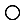 原子有 个。 原子有 个。 图中:●表示D原子,  表示C原子, 表示C原子, 表示镁原子 表示镁原子(4)(已知  =1.414)CXO晶体晶胞结构为NaCl型,由于晶体缺陷,x值为0.88,晶胞边长为4.28×10-10m。晶胞中两个C原子之间的最短距离为___________m(精确至0.01)。若晶体中的C分别为C2﹢、C3﹢,此晶体中C2﹢与C3﹢的最简整数比为_________。 =1.414)CXO晶体晶胞结构为NaCl型,由于晶体缺陷,x值为0.88,晶胞边长为4.28×10-10m。晶胞中两个C原子之间的最短距离为___________m(精确至0.01)。若晶体中的C分别为C2﹢、C3﹢,此晶体中C2﹢与C3﹢的最简整数比为_________。 |
参考解答
、(1)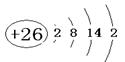 a (2) 3d54s1 s和ds区 a (2) 3d54s1 s和ds区 (3) 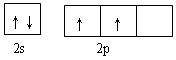 MgCNi3 12 MgCNi3 12(4)3.03×10-10m(2分) 8:3(2分) |
| 根据元素的结构和性质可知,A、B、C、D 四种元素分别是Fe、Cr、Ni、C。 (1)铁的原子序数为26,所以Fe的原子结构示意图为 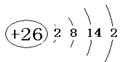 。根据甲和乙的结构可知,选项a正确,答案选a。 。根据甲和乙的结构可知,选项a正确,答案选a。(2)根据构造原理可知,Cr原子的基态的外围电子排布式3d54s1。B同周期且基态原子最外层电子数与B相同的元素是K或铜,分别位于s区和ds区。 (3)根据构造原理可知,碳原子的外围电子排布图是  。根据晶胞结构可知镁原子个数是8×1/8=1,Ni原子个数是6×1/2=3,碳原子在中心,全部属于该晶胞,属于化学式为MgCNi3 。晶体中每个镁原子周围距离最近的Ni原子有3×8÷2=12。 。根据晶胞结构可知镁原子个数是8×1/8=1,Ni原子个数是6×1/2=3,碳原子在中心,全部属于该晶胞,属于化学式为MgCNi3 。晶体中每个镁原子周围距离最近的Ni原子有3×8÷2=12。(4)根据氯化钠的晶胞可知,晶胞中两个Ni原子之间的最短距离为  ×(4.28×10-10m÷2)=3.03×10-10m。设晶体中C2﹢与C3﹢的个数分别是a和b,则2a+3b=2,a+b=0.88,解得a=0.64,b=0.24,所以晶体中C2﹢与C3﹢的最简整数比为8:3。 ×(4.28×10-10m÷2)=3.03×10-10m。设晶体中C2﹢与C3﹢的个数分别是a和b,则2a+3b=2,a+b=0.88,解得a=0.64,b=0.24,所以晶体中C2﹢与C3﹢的最简整数比为8:3。 |
相似问题
下列叙述不正确的是( )A 金刚石晶胞()中平均含有的碳原子数 碘晶体晶胞中平均含有的原子数均为8B
下列叙述不正确的是()A金刚石晶胞()中平均含有的碳原子数、碘晶体晶胞中平均含有的原子数均为8B二氧化硅晶体中最小环上的氧原子数、氯化铯晶体中氯离
下列说法正确的是( )A.有些物质是由分子直接构成的 如二氧化碳 二氧化硅;有些物质是由原子直接构成
下列说法正确的是()A.有些物质是由分子直接构成的,如二氧化碳、二氧化硅;有些物质是由原子直接构成,如金刚石、晶体硅;有些是由离子直接构成的,如
下列说法中 正确的是( )A.构成分子晶体的微粒一定含有共价键B.在结构相似的情况下 原子晶体中的
下列说法中,正确的是( )A.构成分子晶体的微粒一定含有共价键B.在结构相似的情况下,原子晶体中的共价键越强,晶体的熔、沸点越高C.某分子晶体的熔
在40GPa高压下 用激光器加热到1 800 K时 人们成功制得了原子晶体干冰 其结构和性质与SiO
在40GPa高压下,用激光器加热到1 800 K时,人们成功制得了原子晶体干冰,其结构和性质与SiO2原子晶体相似。下列有关推断不正确的是 ( )A.原子晶体干
金属的下列性质中 不能用金属的电子气理论加以解释的是A.易导热B.易导电C.只能作还原剂D.有延展性
金属的下列性质中,不能用金属的电子气理论加以解释的是A.易导热B.易导电C.只能作还原剂D.有延展性












