硫酸工厂排放的尾气中 含少量的二氧化硫。为防止其污染大气 在排放前必需进行尾气处理并设法进行综合利用
| 硫酸工厂排放的尾气中,含少量的二氧化硫。为防止其污染大气,在排放前必需进行尾气处理并设法进行综合利用。 (1)硫酸工厂排放尾气中的SO2通常用足量石灰水吸收,然后再用稀硫酸处理。 ①写出上述过程的化学反应方程式:_________, ②请说出这种尾气处理方法的优点(说出两点即可):___________; ③若某硫酸厂每天排放的1万米3(标准状况)尾气中含0.2%(体积百分数)的SO2,通过上述方法处理,理论上需生石灰_______kg。 (2)近闻美国和日本正在研究用Na2SO3吸收法作为治理SO2污染的一种新方法,该方法: 第一步是用Na2SO3水溶液吸收SO2, 第二步是加热吸收溶液,可得到含高浓度SO2的水蒸气副产品。 这种尾气处理方法与(1)相比的优点是____________。 (3)某研究小组用NaOH溶液吸收尾气中的二氧化硫,将所得的Na2SO3溶液进行电解循环再生,这种新工艺叫再生循环脱硫法;其中阴阳膜组合循环再生机理如下图,a,b离子交换膜将电解槽分为三个区域,电极材料为石墨。 |
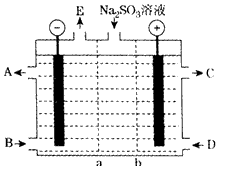 |
| ①图中a表示____(填“阴”或“阳”)离子交换膜。A~E分别代表生产中的原 料或产品,其中C为硫酸,则A表示_______,E表示________。 ②阳极的电极反应式为____。 |
参考解答
| (1)①SO2 +Ca(OH)2=CaSO3↓+H2O ,CaSO3+H2SO4=CaSO4+SO2↑+H2O ②原料生石灰、硫酸价格便宜且容易获得,可得到石膏副产品,产生的SO2含量较高可返回作为原料 ③50 (2) Na2SO3 可循环使用 (3)①阳 ;NaOH溶液 ;氢气 ;②SO32- -2e-+H2O=2H++SO42- |
相似问题
近年来 加“碘”食盐较多使用了碘酸钾(KIO3) KIO3在工业上可用电解法制取 以石墨和铁为电极
近年来,加“碘”食盐较多使用了碘酸钾(KIO3),KIO3在工业上可用电解法制取,以石墨和铁为电极,以KI溶液为电解液在一定条件下电解,反应方程式为KI+H2O
下列实验“操作和现象”与“结论”对应关系正确的是[ ]操作和现象结论A.处理锅炉水垢中的Ca
下列实验“操作和现象”与“结论”对应关系正确的是[ ]操作和现象结论A 处理锅炉水垢中的CaSO4时,依次加入饱和Na2CO3溶液和盐酸,水垢溶解溶解度: S(
按规定在食盐中添加一定量的碘化钾(KIO3)即成为可以为人体补充碘元素的“加碘食盐”.KIO3可用在
按规定在食盐中添加一定量的碘化钾(KIO3)即成为可以为人体补充碘元素的“加碘食盐”.KIO3可用在一定温度下电解KI水溶液的方法制得.以下关于这一生产
以石墨棒作电极 电解氯化铜溶液 若电解时转移的电子数是3.01×1023 则此时在阴极上析出铜的质量
以石墨棒作电极,电解氯化铜溶液,若电解时转移的电子数是3 01×1023,则此时在阴极上析出铜的质量是( )A.8gB.16gC.32gD.64g
利用如图所示装置模拟电解原理在工业生产上的应用.下列说法正确的是( )A.氯碱工业中 X电极上反应
利用如图所示装置模拟电解原理在工业生产上的应用.下列说法正确的是( )A.氯碱工业中,X电极上反应式是4OH-4e-=2H2O+O2↑B.电解精炼铜时,Z溶液中












