将5.6g铁放入121.6g稀盐酸中恰好完全反应。求:(1)生成氢气的质量。(2)反应后溶液中溶质的
| 将5.6g铁放入121.6g稀盐酸中恰好完全反应。求: (1)生成氢气的质量。 (2)反应后溶液中溶质的质量分数。 |
参考解答
| 解:设5.6g铁放入121.6g稀盐酸中生成氢气质量为X,同时生成氯化亚铁的质量为Y 则:Fe+2HCl═=FeCl2+H2↑ 56 127 2 5.6g Y X 根据: 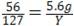 解得Y=12.7g 解得Y=12.7g根据: 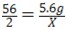 解得X=0.2g 解得X=0.2g(1)生成氢气质量为0.2g; (2)反应后所得溶液的质量为:5.6g+121.6g﹣0.2g=127g 所以反应后溶液中溶质的质量分数为: 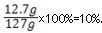 |
相似问题
为了测定某铜锌合金中锌的质量分数 某同学利用该合金与稀硫酸反应 进行了三次实验 所有相关的实验数据记
为了测定某铜锌合金中锌的质量分数,某同学利用该合金与稀硫酸反应,进行了三次实验,所有相关的实验数据记录如下表(实验中误差忽略不计)请计算此合金
已知烧杯中装有200g硫酸和硫酸锌混合溶液 其中含硫酸锌12.1g。向烧杯中逐渐加入锌粒 放出气体质
已知烧杯中装有200g硫酸和硫酸锌混合溶液,其中含硫酸锌12 1g。向烧杯中逐渐加入锌粒,放出气体质量与加入锌粒质量的关系如下图所示。当恰好完全反应时,
某治疗胃酸过多的药物说明书中标注:每片含氢氧化铝250 mg。为判断该药物中氢氧化铝的含量是否属实
某治疗胃酸过多的药物说明书中标注:每片含氢氧化铝250 mg。为判断该药物中氢氧化铝的含量是否属实,进行如下操作:取一片药片,研碎后滴加溶质质量分数
要制得148gCa(OH)2 需要多少克CaO与足量的水反应?
要制得148gCa(OH)2,需要多少克CaO与足量的水反应?
工业上生产的生石灰里常混有少量碳酸钙(不含其它杂质)。为测定生石灰中氧化钙的纯度 取50g样品 在高
工业上生产的生石灰里常混有少量碳酸钙(不含其它杂质)。为测定生石灰中氧化钙的纯度,取50g样品,在高温条件下完全反应,生成2 2g气体,则样品中氧化钙












