由H2和Cl2组成的混合气体 经光照充分反应后 通入到100 mL 1 mol·L-1的NaOH溶液
由H2和Cl2组成的混合气体,经光照充分反应后,通入到100 mL 1 mol·L-1的NaOH溶液中,图A表示溶液中某种离子的物质的量随着通入气体体积的变化而变化的曲线,图B表示溶液中的导电性随着通入气体体积的变化而变化的曲线。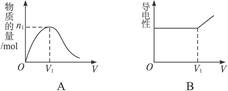 (1)图A表示溶液中_____________________________离子的变化曲线,说明曲线下降的原因:____________________________________________________________________________。 (2)对溶液进行导电性实验,当通入的混合气体体积大于V1时,引起溶液导电性明显增强的主要阳离子是___________。 (3)当n="0.02" mol时,光照前的混合气体中H2和Cl2的物质的量之比为___________。 |
参考解答
(1)ClO- 当通入的气体开始过量时,溶液呈酸性,发生反应:H++ClO- HClO,使n(ClO-)减少 HClO,使n(ClO-)减少(2)H+ (3)3∶5 |
混合气体中H2和Cl2的物质的量之比可以等于1∶1,或大于1∶1,或小于1∶1,只有当小于1∶1时,混合气体经光照充分反应后,通入到NaOH溶液中发生反应:HCl+NaOH====NaCl+H2O,Cl2+2NaOH====NaCl+NaClO+H2O,过量的HCl与NaClO反应生成HClO和NaCl,n(ClO-)才先增后减。但是,由于ClO-+H+ HClO,n(ClO-)不会减少到为0,n(ClO-)='0.02' mol,依据方程式: HClO,n(ClO-)不会减少到为0,n(ClO-)='0.02' mol,依据方程式:Cl2+2NaOH='===NaCl+NaClO' +H2O, 0.02 mol 0.04 mol 0.02 mol NaOH mol+HCl====NaCl+H2O, (0.1-0.04) 0.06 mol H2 + Cl2 ='=== ' 2HCl, 0.03 mol 0.03 mol 0.06 mol, 因此光照前的混合气体中H2和Cl2的物质的量之比为0.03 mol∶(0.02 mol+0.03 mol)=3∶5。 |
相似问题
已知SnCl4 SiCl4 AlCl3 PCl3等氯化物在潮湿的空气中打开瓶塞后 都有白雾生成.为清
已知SnCl4、SiCl4、AlCl3、PCl3等氯化物在潮湿的空气中打开瓶塞后,都有白雾生成.为清楚地观察磷在Cl2中燃烧,达到PCl3和PCl5分步生成的目的.可预先把
下列反反应发生时 会产生红棕色烟的是( )A.钠在氯气中燃烧B.铜在氯气中燃烧C.氢气在氯气中燃烧
下列反反应发生时,会产生红棕色烟的是( )A.钠在氯气中燃烧B.铜在氯气中燃烧C.氢气在氯气中燃烧D.铁在氯气中燃烧
为测定氯水的物质的量浓度 在100 mL氯水中加入足量的碘化钾溶液 把游离出来的碘单质按下述反应进行
为测定氯水的物质的量浓度,在100 mL氯水中加入足量的碘化钾溶液,把游离出来的碘单质按下述反应进行定量分析,耗去300 mL、1 mol L的硫代硫酸钠(Na2S
对三硫化四磷分子的结构研究表明 该分子中没有不饱和键 且各原子的最外层均已达到了 8 个电子的结构。
对三硫化四磷分子的结构研究表明,该分子中没有不饱和键,且各原子的最外层均已达到了 8 个电子的结构。则一个三硫化四磷分子中含有的共价键个数是A.7
二氯化二硫(S2Cl2)在工业上用于橡胶的硫化.为在实验室合成S2Cl2 某化学研究性学习小组查阅了
二氯化二硫(S2Cl2)在工业上用于橡胶的硫化.为在实验室合成S2Cl2,某化学研究性学习小组查阅了有关资料,得到如下信息:①将干燥的氯气在110℃~140℃












