已知1 mol CuSCN在下列反应中失去7 mol电子 完成并配平下列化学反应方程式:CuSCN+
| 已知1 mol CuSCN在下列反应中失去7 mol电子,完成并配平下列化学反应方程式:CuSCN+KMnO4+H2SO4——HCN+CuSO4+MnSO4+K2SO4+H2O |
参考解答
| 10CuSCN+14KMnO4+21H2SO4====10HCN+10CuSO4+14MnSO4+7K2SO4+16H2O |
观察反应前后Mn的化合价变化: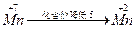 设CuSCN的化学计量数为x,KMnO4的化学计量数为y,根据得失电子的总数相等,则7x=5y,即x∶y=5∶7,代入后用观察法确定其他物质的化学计量数,最后使各项化学计量数变为整数,得:10、14、21、10、10、14、7、16。 |
相似问题
在S2- Fe2+ Mg2+ S I- H+ Fe3+中 只有氧化性的是_________;只有还原
在S2-、Fe2+、Mg2+、S、I-、H+、Fe3+中,只有氧化性的是_________;只有还原性的是_________;既有氧化性又有还原性的是_________。
已知亚甲基蓝其氧化型呈蓝色 还原型呈无色 其转化关系式为:氧化型(蓝色)+ne-还原型(无色) 奇妙
已知亚甲基蓝其氧化型呈蓝色,还原型呈无色,其转化关系式为:氧化型(蓝色)+ne-还原型(无色),奇妙的“蓝瓶子”实验就是利用上述原理,其装置如图1。图1图2某
已知下列反应:2FeCl3+2KI===2FeCl2+2KCl+I22FeCl2+Cl2===2Fe
已知下列反应:2FeCl3+2KI===2FeCl2+2KCl+I22FeCl2+Cl2===2FeCl3I2+SO2+2H2O===H2SO4+2HI判断下列物质的还原性由强到弱的顺序是A.I->Fe2+>Cl-
黑火药的爆炸反应为:2KNO3+S+3C=K2S+N2↑+3CO2↑ 其中被还原的元素是( )A.
黑火药的爆炸反应为:2KNO3+S+3C=K2S+N2↑+3CO2↑,其中被还原的元素是()A.NB.CC.N和SD.N和C
菜谱中记载:河虾不宜与西红柿同食.主要原因是河虾中含有五价砷 西红柿中含有比较多的维生素C 两者同食
菜谱中记载:河虾不宜与西红柿同食.主要原因是河虾中含有五价砷,西红柿中含有比较多的维生素C,两者同食时会生成有毒的三价砷.下列说法正确的是(












