某反应中反应物与生成物有:AsH3 H2SO4 KBrO3 K2SO4 H3AsO4 H2O和一种
| 某反应中反应物与生成物有:AsH3、H2SO4、 KBrO3、K2SO4、H3AsO4、H2O和一种未知物质X。 (1)已知KBrO3在反应中得到电子,则该反应的还原剂是_______________。 (2)已知0.2mol KBrO3在反应中得到l mol电子生成X,则X的化学式为__________ (3)根据上述反应可推知___________ a氧化性:KBrO3> H3AsO4 b氧化性:H3AsO4> KBrO3 c还原性:AsH3>x d还原性:x> AsH3 (4)将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,并标出电子转移的方向和数目 |
 |
参考解答
| (1)AsH3 (2)Br2 (3)ac |
(4)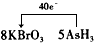 |
相似问题
下列变化需要加入还原剂才能实现的是[ ]A.CaCO3→CO2 B.Fe3+→Fe2+C.C
下列变化需要加入还原剂才能实现的是[ ]A.CaCO3→CO2 B.Fe3+→Fe2+C.Cl2→ClO- D.SO42-→BaSO4
下列反应中 氧化剂与还原剂物质的量的关系为1∶2的是 [ ]A N2O+4H2==2NH3
下列反应中,氧化剂与还原剂物质的量的关系为1∶2的是[ ]A、N2O+4H2==2NH3+H2O B、2CH3COOH+Ca(ClO)2==2HClO+Ca(CH3COO)2 C、I2+2NaClO3==2NaIO3+Cl2 D、4HCl+MnO2==MnCl2+Cl2↑+2H2O
Na3N是离子化合物 它和水作用可产生NH3 下列说法正确的是 [ ]A.Na+和N3-的
Na3N是离子化合物,它和水作用可产生NH3,下列说法正确的是 [ ]A.Na+和N3-的电子层结构都与氩原子相同 B.Na3N与盐酸反应可生成两种盐C.Na+的半径大
下列是某学生总结的一些规律 其中正确的是 [ ]A.一种元素可能有多种氧化物 但是同种化合价
下列是某学生总结的一些规律,其中正确的是 [ ]A.一种元素可能有多种氧化物,但是同种化合价只对应一种氧化物B.酸性氧化物都可以与碱反应,生成盐和
下列反应中 水作为还原剂的是[ ]A. 2Na+2H2O==2NaOH+H2↑B. Cl2+
下列反应中,水作为还原剂的是[ ]A 2Na+2H2O==2NaOH+H2↑B Cl2+H2OHCl+HClOC 2F2+2H2O==4HF+O2 D SO2+H2OH2SO3












