LiAlH4是重要的储氢材料 其组成类似于Na3AlF6。常见的供氢原理如下面两个方程式所示:①2L
| LiAlH4是重要的储氢材料,其组成类似于Na3AlF6。常见的供氢原理如下面两个方程式所示: ①2LiAlH4 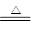 2LiH+2Al+3H2↑ 2LiH+2Al+3H2↑②LiAlH4+2H2O=LiAlO2+4H2↑ 下列说法正确的是( )
|
参考解答
| C |
| A项,LiAlH4由Li+、AlH4—构成,它是离子化合物,错误;B项,反应①中生成3 mol氢气时,转移6 mol电子,反应②中生成4 mol氢气时,转移4 mol电子,生成等量氢气时转移电子数之比为21,错误;C项,氢化锂具有强还原性,与水发生归中反应生成氢气,正确;D项,氢气所处温度和压强不确定,不一定是标准状况,所以无法计算铝的质量,错误。 点拨:本题考查化合物的分类、氧化还原反应原理及简单计算等,意在考查考生将实际问题分解,通过运用相关知识,采用分析、综合的方法,解决简单化学问题的能力。 |
相似问题
FeS2可在Fe2(SO4)3溶液中“溶解” 硫元素都以SO42-的形式存在。若有l mol FeS
FeS2可在Fe2(SO4)3溶液中“溶解”,硫元素都以SO42-的形式存在。若有l mol FeS2“溶解”,则生成H2SO4的物质的量为A.2molB.4 molC.6 molD.8 mol
PbO2是褐色固体 受热分解为Pb的+4和+2+4价的混合氧化物 +4价的Pb能氧化浓盐酸生成Cl
PbO2是褐色固体,受热分解为Pb的+4和+2+4价的混合氧化物,+4价的Pb能氧化浓盐酸生成Cl2;现将1mol PbO2加热分解得到O2,向剩余固体中加入足量的浓盐
氮化硅(Si3N4)是一种新型陶瓷材料 它可由石英与焦炭在高温的氮气流中 通过以下反应制得:3SiO
氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2+6C+2N2Si3N4+6CO。下列叙述正确的是A.Si3N4的摩尔质
将18 g铜和铁的混合物投入200 mL稀硝酸中 充分反应后得到标准状况下2.24 L NO 剩
将18 g铜和铁的混合物投入200 mL稀硝酸中,充分反应后得到标准状况下2 24 L NO,剩余9 6 g金属;继续加入200 mL等浓度的稀硝酸,金属完全溶解,又
某离子反应中涉及H2O ClO— NH4+ H+ N2 Cl—六种微粒。其中N2的物质的量随时间变化
某离子反应中涉及H2O、ClO—、NH4+、H+、N2、Cl—六种微粒。其中N2的物质的量随时间变化的曲线如右图所示。下列判断正确的是:A该反应的还原剂是Cl—B消












