用Na2SO3还原 如果还原含有2.4×10-3 mol 的溶液时 消耗30 mL 0.2 mol·
用Na2SO3还原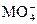 ,如果还原含有2.4×10-3 mol ,如果还原含有2.4×10-3 mol 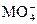 的溶液时,消耗30 mL 0.2 mol·L-1 Na2SO3溶液,则Mn元素在还原产物中的化合价为( ) 的溶液时,消耗30 mL 0.2 mol·L-1 Na2SO3溶液,则Mn元素在还原产物中的化合价为( )
|
参考解答
| B |
S化合价+4 +6,升,失6×10-3 mol×2e-; +6,升,失6×10-3 mol×2e-;Mn化合价+7  x,降,得2.4×10-3mol×(7-x)e-; x,降,得2.4×10-3mol×(7-x)e-;得失电子相等6×10-3×2e-=2.4×10-3×(7-x)e-;x=2。 |
相似问题
黑火药的爆炸反应方程式可表示为:2KNO+S+3CKS+N↑+3CO↑其中氧化剂是( )A.CB.K
黑火药的爆炸反应方程式可表示为:2KNO+S+3CKS+N↑+3CO↑其中氧化剂是()A.CB.KNOC.KNO和SD.S
下列铁元素所处的状态既有氧化性又有还原性的物质是( )A.FeB.FeCl2C.FeCl3D.Fe
下列铁元素所处的状态既有氧化性又有还原性的物质是( )A.FeB.FeCl2C.FeCl3D.Fe2O3
需加入适当的还原剂才能实现的反应是( )A.PCl3 → PCl5B.MnO2 → Mn2+C.S
需加入适当的还原剂才能实现的反应是( )A.PCl3 → PCl5B.MnO2 → Mn2+C.SO2 → SO3D.Fe2O3→ Fe
下列反应中不属于氧化还原反应的是( )A.Cl2+H2O====HCl+HClOB.3CO+Fe
下列反应中不属于氧化还原反应的是()A.Cl2+H2O====HCl+HClOB.3CO+Fe2O32Fe+3CO2C.CaCO3+SiO2CaSiO3+CO2↑D.3CuS+8HNO3====3Cu(NO3)2+2NO↑+3S↓+4H2O
生活污水中含有大量的有机和无机含氮化合物 这些过量的含氮化合物会造成水体污染 危害水生生物生存和人类
生活污水中含有大量的有机和无机含氮化合物,这些过量的含氮化合物会造成水体污染,危害水生生物生存和人类的健康。脱氮是污水处理的重要内容之一,其实












