A B C D E为中学化学常见的单质或化合物 其相互转化关系如下图所示。(1)若A是淡黄色化合物;
A、B、C、D、E为中学化学常见的单质或化合物,其相互转化关系如下图所示。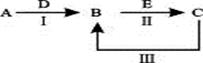 (1)若A是淡黄色化合物;常温下D是无色气体;C中含有的阴、阳离子均为10电子粒子。 ①写出反应A→B的化学方程式 ; ②将一定量的气体D通入2 L C的溶液中,向所得溶液中边逐滴加入稀盐酸边振荡至过量,产生的气体与盐酸物质的量的关系如图(忽略气体的溶解和HCl的挥发)。请回答:O点溶液中所含溶质的化学式为 ,a点溶液中各离子浓度由大到小的关系是 。 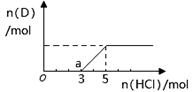 (2)若将(1)中的气体D通入氢氧化钡溶液中得不溶物F,F的KSP=8.1×10-9。现将该沉淀放入0.1mol/L 的BaCl2溶液中,其KSP ,(填:增大、减小或不 变),组成不溶物F的阴离子在溶液中的浓度为 mol/L。 |
参考解答
| (1)2CO2 + 2Na2O2= 2Na2CO3 + O2 (3分)NaOH、Na2CO3 (2分) c(Na+)>c(Cl-)>c(HCO3-)>c(OH-)>c(H+)>c(CO32-) (3分) (2)不变 (2分) ; 8.1×10-8 (2分) |
试题分析:由题意结合关系图确定A为过氧化钠,B为碳酸钠,C为氢氧化钠,所以A→B化学方程式为2CO2 + 2Na2O2= 2Na2CO3 + O2;由碳酸钠与盐酸反应的特点Na2CO3+HCl=NaHCO3+NaCl,NaHCO3+HCl=NaCl+H2O+CO2↑两步消耗相同量的盐酸,所以确定图中O点的溶质为NaOH、Na2CO3 ;a 点为3molNaCl和2molNaHCO3,离子浓度大小为 c(Na+)>c(Cl-)>c(HCO3-)>c(OH-)>c(H+)>c(CO32-) ;Ksp只受温度影响,所以不变,而c(SO42-)=Ksp(BaSO4)/c(Ba2+)=8.1×10-8. |
相似问题
下列实验能成功的是( )。①用灼烧法鉴别Na2CO3固体和NaHCO3固体 ②用观察法区别Na2O
下列实验能成功的是( )。①用灼烧法鉴别Na2CO3固体和NaHCO3固体 ②用观察法区别Na2O粉末和Na2O2粉末 ③用AlCl3溶液鉴别Na2CO3溶液和NaOH溶液 ④
一般测定样品中成分含量的实验应重复2~3次。为了测定某氢氧化钠固体中混有的碳酸钠的质量分数 甲 乙
一般测定样品中成分含量的实验应重复2~3次。为了测定某氢氧化钠固体中混有的碳酸钠的质量分数,甲、乙、丙三位同学分别设计了如下实验方案:Ⅰ 甲同学的
钠和铝是两种重要的金属。请回答(1)将一小块金属钠投入水中 可观察到的实验现象是__________
钠和铝是两种重要的金属。请回答(1)将一小块金属钠投入水中,可观察到的实验现象是_____________(填序号)。a.钠沉到水底 b.钠熔成小球 c.小球四
A B C均为中学常见的单质或化合物 一定条件下 存在转化关系:A + H2O → B + C 。下
A、B、C均为中学常见的单质或化合物,一定条件下,存在转化关系:A + H2O → B + C 。下列说法正确的是A.若B为强碱,则A一定为金属钠 B.若B为
下列说法正确的是( )A.金属钠在空气中燃烧的火焰呈黄色 是因为生成的Na2O2为淡黄色固体B.铁
下列说法正确的是( )A.金属钠在空气中燃烧的火焰呈黄色,是因为生成的Na2O2为淡黄色固体B.铁丝在Cl2中燃烧有红棕色的烟,是因为生成的FeCl3为红棕












