某溶液中可能含有碳酸钠 硫酸钠 氯化钾 盐酸中的一种或几种 为测定其成分 进行如下实验。第一步:取样
| 某溶液中可能含有碳酸钠、硫酸钠、氯化钾、盐酸中的一种或几种,为测定其成分,进行如下实验。 第一步:取样,进行焰色反应,透过蓝色钴玻璃观察到火焰呈紫色。 第二步:另取样,先后逐滴加入氯化钡溶液、稀硝酸,产生沉淀的物质的量与时间的关系如下图所示。 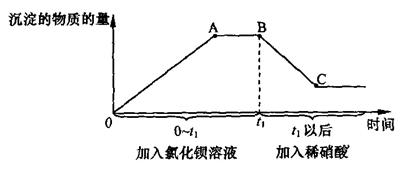 (1)由上述实验可知,原溶液中一定含有碳酸钠、硫酸钠和___________. (2)第二步实验中,AB之间图像所对应的溶液中的溶质一定有________. (3)BC段减少的沉淀是__________________. (4)C点沉淀的物质的量为B点沉淀的物质的量的三分之一。原溶液中碳酸钠的物质的量(m1)与硫酸钠的物质的量(n2)的关系为m1=_______________。 |
参考解答
| (1)KCl或氯化钾(2)NaCl、BaCl2、KCl或氯化钠、氯化钡、氯化钾 (3)BaCO3或碳酸钡(4)2n2 |
| (1)“焰色反应,透过蓝色钴玻璃观察到火焰呈紫色“可说明溶液中含钾,即含氯化钾。 加入氯化钡产生沉淀,说明可能含硫酸钠或碳酸钠。然后加入稀硝酸,沉淀部分溶解,则沉淀中未溶解的沉淀应为硫酸钡,则原来一定含硫酸钠;溶解的沉淀是碳酸钡,则原来一定含碳酸钠。所以原溶液中一定含硫酸钠、碳酸钠和氯化钾。 (2)A点是生成沉淀质量最大值的点,即A点表示碳酸钠和硫酸钠恰好与氯化钡完全反应。则AB段则表示氯化钡过量。
(3)Na2CO3与BaCl2反应生成碳酸钡沉淀,Na2SO4与BaCl2反应生成硫酸钡沉淀; 其中碳酸钡沉淀可与稀硝酸反应生成硝酸钡、水和二氧化碳;所以BC段减少的沉淀是碳酸钡。 (4)C点时,碳酸钡沉淀全部反应,剩余的未反应的沉淀应为硫酸钡。据“C点沉淀的物质的量为B点沉淀的物质的量的三分之一”,即BC段减少的沉淀(碳酸钡)的物质的量占三分之二,C点沉淀(硫酸钡)的物质的量占三分之一。根据碳酸钡的物质的量=碳酸钠的物质的量;硫酸钡的物质的量=硫酸钠的物质的量。所以m1=2n2 点评:本题考查了物质间的反应,先根据实现现象推出原溶液的成分,现根据图像推出碳酸钠与硫酸钠的物质的量的比。 |
相似问题
如图所示的是初中常见物质之间的反应及转化关系(部分生成物省略) 其中 甲 乙 丙 丁 戊都是氧化物
如图所示的是初中常见物质之间的反应及转化关系(部分生成物省略),其中 甲、乙、丙、丁、戊都是氧化物,A和B组成元素相同,乙和丙组成元素相同且常温
鉴别日常生活中的下列各组物质 其操作不正确的是 A.软水和硬水:滴加肥皂水B.氧气和二氧化碳:滴
鉴别日常生活中的下列各组物质,其操作不正确的是A.软水和硬水:滴加肥皂水B.氧气和二氧化碳:滴加澄清石灰水C.氮气和二氧化碳:伸入燃着的木条D.水
甲 乙 丙 丁均为初中化学常见物质 它们有如下图所示的转化关系。请据图回答问题。(1)若丙为最清洁的
甲、乙、丙、丁均为初中化学常见物质,它们有如下图所示的转化关系。请据图回答问题。(1)若丙为最清洁的气体燃料,则丙的化学式为。 请写出一个符合上
下列物质的鉴别方法正确的是
下列物质的鉴别方法正确的是A.用澄清石灰水鉴别氢气和一氧化碳B.用酚酞鉴别碳酸钠溶液和氢氧化钠溶液C.用食盐水鉴别硬水和软水D.用水鉴别硝酸铵固体
为除去下表样品中的少量杂质(括号内为杂质) 所选试剂及操作方法均正确的是序号样品成分所选试剂操作方法
为除去下表样品中的少量杂质(括号内为杂质),所选试剂及操作方法均正确的是序号样品成分所选试剂操作方法AKCl(MnO2)水溶解、过滤、洗涤干燥BNa2CO3(












