氯气常用于自来水厂杀菌消毒。(1)工业上用铁电极和石墨做为电极电解饱和食盐水生产氯气 铁电极作
| 氯气常用于自来水厂杀菌消毒。 (1)工业上用铁电极和石墨做为电极电解饱和食盐水生产氯气,铁电极作 极,石墨电极上的电极反应式为 。 (2)氯氧化法是在碱性条件下,用Cl2将废水中的CN-氧化成无毒的N2和CO2。该反应的离子方程式为 。 (3)氯胺(NH2Cl)消毒法是在用液氯处理自来水的同时通入少量氨气,发生反应:Cl2 + NH3 = NH2Cl + HCl,生成的NH2Cl比HClO稳定,且能部分水解重新生成HClO,起到消毒杀菌的作用。 ①氯胺能消毒杀菌的原因是 (用化学用语表示)。 ②氯胺消毒法处理后的水中,氮元素多以NH4+的形式存在。 已知:NH4+(aq) + 1.5O2(g)= NO2-(aq) + 2H+(aq) + H2O (l) ΔH=-273 kJ·mol-1 NH4+(aq) + 2O2(g)= NO3-(aq) + 2H+(aq) + H2O (l) ΔH =-346 kJ·mol-1 NO2-(aq)被O2氧化成NO3-(aq)的热化学方程式为 。 (4)在水产养殖中,可以用Na2S2O3将水中残余的微量Cl2除去,某实验小组利用下图所示装置和药品制备Na2S2O3。 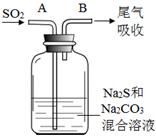 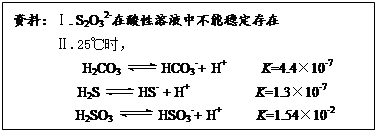 结合上述资料回答: 开始通SO2时,在B口检测到有新的气体生成,判断从B口排出的气体中是否含有H2S,并写出判断依据 。 为获得较多的Na2S2O3,当溶液的pH接近7时,应立即停止通入SO2,其原因是 。 |
参考解答
| (1)阴 2Cl- - 2e- = Cl2↑ (2)5Cl2 + 2CN- + 4H2O = 10Cl- + N2↑+ 2CO2↑+ 8H + (3)① NH2Cl+ H2O  NH3 + HClO(不写可逆号扣1分) NH3 + HClO(不写可逆号扣1分)② 2NO2- (aq) + O2(g) = 2NO3-(aq) ΔH = -146 kJ·mol-1(反应热写错扣1分) (4)①答案1:含H2S,由电离常数知H2SO3酸性强于H2S,溶液中的S2-与H2SO3反应生成H2S。 答案2:不含H2S,S2-还原性较强,能被SO2氧化生成其它含硫物质。 (只写“含”或“不含”为0分) ②通入过多SO2会使溶液的pH小于7,S2O32-在酸性溶液中不能稳定存在。 |
试题分析:(1)工业上用铁电极和石墨做为电极电解饱和食盐水生产氯气,铁电极不能做阳极,如果做阳极,Fe-2e- 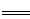 Fe2+,不会得到氯气,所以铁电极作阴极,石墨电极上的电极反应式为2Cl- - 2e- = Cl2↑。 Fe2+,不会得到氯气,所以铁电极作阴极,石墨电极上的电极反应式为2Cl- - 2e- = Cl2↑。(2)氯氧化法是在碱性条件下,用Cl2将废水中的CN-氧化成无毒的N2和CO2。 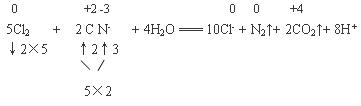 (3)①氯胺能消毒杀菌的原因是发生了水解NH2Cl+ H2O  NH3 + HClO,HClO具有强氧化性,能消毒杀菌。 NH3 + HClO,HClO具有强氧化性,能消毒杀菌。②NH4+(aq) + 1.5O2(g)= NO2-(aq) + 2H+(aq) + H2O (l) ΔH=-273 kJ·mol-1 ① NH4+(aq) + 2O2(g)= NO3-(aq) + 2H+(aq) + H2O (l) ΔH =-346 kJ·mol-1 ② ②×2-①×2得NO2-(aq)被O2氧化成NO3-(aq)的热化学方程式为 2NO2- (aq) + O2(g) = 2NO3-(aq) ΔH = -146 kJ·mol-1; (4)①开始通SO2时,在B口检测到有新的气体生成,判断从B口排出的气体中是否含有H2S,答案1:含H2S,由电离常数知H2SO3酸性强于H2S,溶液中的S2-与H2SO3反应生成H2S。 答案2:不含H2S,S2-还原性较强,能被SO2氧化生成其它含硫物质。 ②为获得较多的Na2S2O3,当溶液的pH接近7时,应立即停止通入SO2,其原因是通入过多SO2会使溶液的pH小于7,S2O32-在酸性溶液中不能稳定存在。 |
相似问题
下列离子方程式书写正确的是A.向Ba(OH)2溶液中滴加NaHSO4溶液至中性:Ba2++H++OH
下列离子方程式书写正确的是A.向Ba(OH)2溶液中滴加NaHSO4溶液至中性:Ba2++H++OH—+SO42—=BaSO4↓+H2OB.用铜作电极电解硫酸溶液:2H2O2H2↑+O2↑C.向
下列表示对应化学反应的离子方程式正确的是A.MnO2固体与浓盐酸反应制取Cl2:MnO2+4HClM
下列表示对应化学反应的离子方程式正确的是A.MnO2固体与浓盐酸反应制取Cl2:MnO2+4HClMn2++2Cl-+Cl2↑+2H2OB.AlCl3溶液中滴加浓氨水至过量:Al3++4N
黑火药爆炸时发生多种化学反应 其中主要化学反应方程式为:2KNO3+3C+SK2S+N2↑+3CO2
黑火药爆炸时发生多种化学反应,其中主要化学反应方程式为:2KNO3+3C+SK2S+N2↑+3CO2↑(1)上述反应中,原子半径最小的元素其原子结构示意图为_____
下列图示与对应的叙述相符的是( )A.图Ⅰ表示常温下盐酸滴加到0.1 mol·L-1某碱溶液中得到
下列图示与对应的叙述相符的是()A.图Ⅰ表示常温下盐酸滴加到0 1 mol·L-1某碱溶液中得到的滴定曲线,由图Ⅰ可知二者恰好中和时,所得溶液的pH>7B.
(10分)某科研小组设计出利用工业废酸(l0%)来堆浸某废弃的氧化铜锌矿的方案 实现废物综合利用 如
(10分)某科研小组设计出利用工业废酸(l0%)来堆浸某废弃的氧化铜锌矿的方案,实现废物综合利用,如下图所示。已知:各离子开始沉淀及完全沉淀时的pH如下












