常温下 在溶液中可发生以下反应:①16H++10Z-+2===2X2++5Z2+8H2O ②2M2+
常温下,在溶液中可发生以下反应:①16H++10Z-+2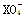 ===2X2++5Z2+8H2O,②2M2++R2===2M3++2R-,③2R-+Z2===R2+2Z-,由此判断下列说法错误的是( ) ===2X2++5Z2+8H2O,②2M2++R2===2M3++2R-,③2R-+Z2===R2+2Z-,由此判断下列说法错误的是( )
|
参考解答
| A |
试题分析:氧化还原反应的方程的左边的氧化剂的氧化性大于右边的氧化剂,还原剂的还原性大于右边的还原剂,根据①16H++10Z-+2 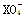 ===2X2++5Z2+8H2O,②2M2++R2===2M3++2R-,③2R-+Z2===R2+2Z-,可以知道M3+<R2<Z2< ===2X2++5Z2+8H2O,②2M2++R2===2M3++2R-,③2R-+Z2===R2+2Z-,可以知道M3+<R2<Z2<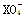 ,故A错误,为正确答案;还原性为X2+<Z-<R-<M2+,故B正确;根据①16H++10Z-+2 ,故A错误,为正确答案;还原性为X2+<Z-<R-<M2+,故B正确;根据①16H++10Z-+2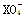 ===2X2++5Z2+8H2O,可以知道,Z的化合价升高,所以被氧化,在③2R-+Z2===R2+2Z-,中,Z元素的化学价降低,被还原,故C正确,根据M3+<Z2,可以得到常温下可发生反应2M2++Z2===2M3++2Z-,所以D也正确,所以本题选A。 ===2X2++5Z2+8H2O,可以知道,Z的化合价升高,所以被氧化,在③2R-+Z2===R2+2Z-,中,Z元素的化学价降低,被还原,故C正确,根据M3+<Z2,可以得到常温下可发生反应2M2++Z2===2M3++2Z-,所以D也正确,所以本题选A。点评:本题考查了氧化还原反应知识,根据给出的化学方程式来判断物质的氧化性,氧化还原反应是高考考查的重点和难点,本题有一定的综合性,难度适中。 |
相似问题
15年前 清华才女朱令离奇铊中毒的事件曾引发一场多年难解的疑案。而在近日 广东东莞一名在电子企业打工
15年前,清华才女朱令离奇铊中毒的事件曾引发一场多年难解的疑案。而在近日,广东东莞一名在电子企业打工的女工也意外出现铊中毒并被家属认为是“职业病
(6分)根据反应(1)2P+5Br2+8H2O=2H3PO4+10HBr (2)Cl2+2HBr=2
(6分)根据反应(1)2P+5Br2+8H2O=2H3PO4+10HBr (2)Cl2+2HBr=2HCl+Br2 (3)2KMn04+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O推断氧化性(氧化
已知2KClO3+I2=2KIO3+Cl2 下列对此反应的说法不正确的是( )A.氧化产物与还原产
已知2KClO3+I2=2KIO3+Cl2,下列对此反应的说法不正确的是( )A.氧化产物与还原产物的物质的量比为2:1B.若在标准状况下产生11 2LCl2,转移电子的物
根据反应式:①2Fe3+ + 2I- = 2Fe2+ + I2 ②Br2 + 2Fe2+ ='==
根据反应式:①2Fe3+ + 2I- = 2Fe2+ + I2②Br2 + 2Fe2+ ="==" 2Fe3+ +2Br-,可判断离子的还原性从强到弱的顺序是A.Br-、Fe2+、I-B.I-
已知反应①2BrO3- + Cl2 =Br2 +2ClO3-②5Cl2 + I2 +6H2O=2HI
已知反应①2BrO3- + Cl2 =Br2 +2ClO3-②5Cl2 + I2 +6H2O=2HIO3 +10HCl③ClO3- +5Cl-+6H+=3Cl2 +3H2O,下列有关氧化(还原)能力强弱顺序正确的












